26.(15分)A、B、C、D、E代表五种原子序数依次增大的元素。已知:
①A、B、C的电子层数之和为6;
②A、B能形成直线形四原子分子;
③C是短周期元素中质子数与最外层电子数之比值最大的元素;
④C、D、E同周期,D单质在适量E单质中燃烧生成两种化合物。
请回答下列问题:
⑴B元素的名称为 ,C元素的符号为 ,D元素的名称为 。
⑵上述五种元素中非金属性最强的是 (填元素符号),写出工业上制备这种元素的单质的离子方程式 。
⑶下述说法中,能说明五种元素中的某种元素具有最强的金属性的是 。
①最高价氧化物水化物的碱性最强
②最高价氧化物水化物的酸性最强
③形成的气态氢化物最稳定
④常温下与冷水反应能置换产生氢气
⑤所形成的化合物中只显正价
⑷五种元素构成的所有单质和化合物中,具有正四面体结构的分子共有 种,其中,一分子中含化学键数目最多的分子是 (填化学式)。
⑸D单质在足量E单质中燃烧的产物能遇水水解生成两种化合物,则该燃烧产物1mol与足量NaOH溶液反应最多能消耗 mol NaOH
|
阳离子 |
K+ |
Al3+ |
Ba2+ |
Mg2+ |
Ag+ |
|
阴离子 |
NO3- |
Cl- |
CO32- |
SO42- |
OH- |
9.将质量分数为0.052(5.2%)的NaOH溶液1 L(密度为1.06 g/cm3),用铂电极电解,当溶液中NaOH的质量分数改变了0.010(1.0%)时停止电解,则这时溶液中应符合的关系是( )
|
|
NaOH的质量分数 |
阳极析出的物质的质量/g |
阴极析出的物质的质量/g |
|
A |
0.062(6.2%) |
19 |
152 |
|
B |
0.062(6.2%) |
152 |
19 |
|
C |
0.042(4.2%) |
1.2 |
9.4 |
|
D |
0.042(4.2%) |
9.4 |
1.2 |
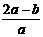 B.
B.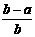 C.
C.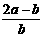 D.
D.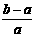
 D.当雨水的pH低于5.6时称为酸雨
D.当雨水的pH低于5.6时称为酸雨