28、(共16分)(1)(8分)某校学生为探究乙二酸(俗称草酸)的部分化学性质,进行了下述实验:
I、 向盛有少量乙二酸饱和溶液的试管中滴入用硫酸酸化的高锰酸钾稀溶液,振荡,观察到的现象为___________________________________, 说明乙二酸具有__________ (填“氧化性”、“还原性”或“酸 性”)。
II、 课本实验设计得简要明了,但也存在一些不足,在探究过程中对其进行分析与改进也是研究性学习的一个重要课题。
已知草酸晶体(H2C2O4·2H2O)受热易分解(分解温度为175℃)产生CO和CO2,下图为高三课本中关于草酸晶体受热分解及验证其部分分解产物的实验装置图。
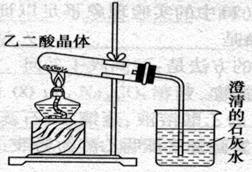
1)写出草酸晶体受热分解的化学方程式_____________________________________.
2)设计该装置欲验证的分解产物是_______________________ 。
3)草酸晶体的某些物理性质如下表:
|
|
分子式 |
颜色、状态 |
水溶性 |
熔点/℃ |
密度/g.cm-3 |
|
草酸晶体 |
H2C2O4·2H2O |
无色晶体 |
易溶于水 |
101.5 |
1.650 |
有的同学认为,用该装置进行实验,存在着不合理因素,请分析指出(任答两点):
① _______________________________________________________________________。
② _______________________________________________________________________。
(2)(8分)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
①定性分析:如图甲可通过观察 ,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3 更为合理,其理由是
写出H2O2在二氧化锰作用下发生反应的化学方程式 。
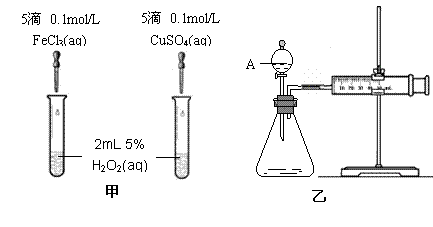
②定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为 ,检查该装置气密性的方法是
,实验中需要测量的数据是 。
10.X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z的最外层电子数是内层电子总数的3倍。下列有关叙述正确的是
A.X肯定为碱金属元素
B.稳定性:Y的氢化物>Z的氢化物
|
D.Y、Z两元素形成的化合物熔点较低
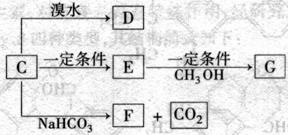
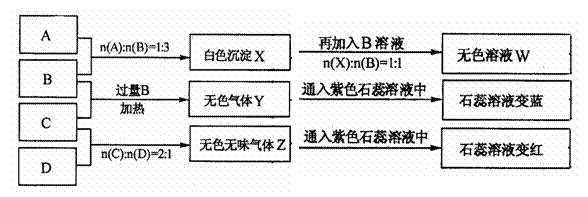
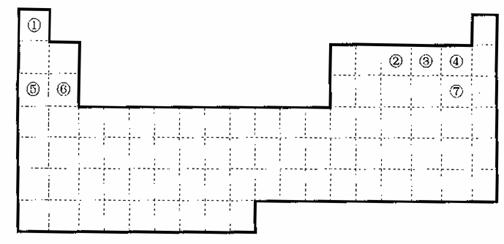
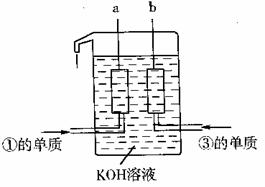 (3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中的原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式
;在一定条件下1g①的单质在足量③的单质中完全燃烧生成液态物质时,放出的热量为akJ,请写出此条件下表示①的单质燃烧热的热化学方程式
(3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中的原子半径最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式
;在一定条件下1g①的单质在足量③的单质中完全燃烧生成液态物质时,放出的热量为akJ,请写出此条件下表示①的单质燃烧热的热化学方程式 2H2O
+ O2↑
2H2O
+ O2↑ 、Na+、Cl-、HCO
、Na+、Cl-、HCO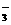
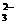
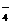 、Al3+、SO
、Al3+、SO