21.(12分)某研究性学习小组的同学拟分析某市空气的质量
情况,测定该市空气中SO2的含量并制定下列研究方案:
I. 资料表明,SO2具有较强的还原性,能与酸性KMnO4溶
液(紫色,其还原产物Mn2+在水溶液中接近无色)发生反应:
5SO2+2MnO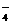 +2H2O=5SO
+2H2O=5SO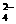 +2Mn2+++4H+
+2Mn2+++4H+
Ⅱ.设计实验方案:
方案一:利用SO2使品红溶液褪色作定性分析。其原理为 ;
方案二:利用SO2的还原性,使SO2和已知浓度及体积的酸性KMnO4溶液反应进行定量分析。
Ⅲ.选择分析地点:某工业区、某公园、某居民小区、某商业区、某交通枢纽。
Ⅳ.选择分析时间:晴天、风速较小时;晴天、风速较大时;雨前;雨后。
V.对测定的结果进行初步分析并向相关单位提出建议。
请你参与该研究性学习小组的活动并发表你的见解:
(1)该小组的同学拟用下列装置通过方案二定量分析空气中SO2的含量:
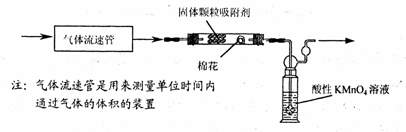
①通人空气前应进行的实验操作是 ;
②当看到实验的现象为 时,应停止通空气;
③实验过程中需测量并记录的数据: 。
(2)下图是该小组同学根据实验测得的县城不同地区空气中SO2含量:
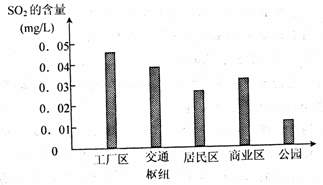
①工厂区、交通枢纽SO2含量明显高于其他地区的原因是 ;
②请你向当地有关部门提出一条减少厂区SO2排放的建议 ;
(3)下表是该小组同学测得的不同天气情况下的县城空气中SO2的平均含量。请你分析
雨后或风速较大时SO2平均含量较低的原因:① ;2 。
|
天气情况 |
平均分速(m/s) |
空气中SO2平均含量(mg/L) |
|
雨前 |
2.0 |
0.03 |
|
雨后 |
2.2 |
0.01 |
|
晴 |
23 |
0.015 |
|
晴 |
0.9 |
0.03 |
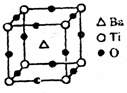 ①偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩
①偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩
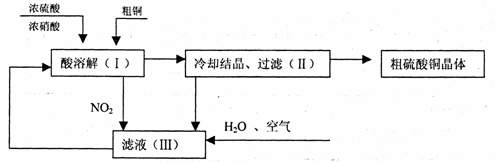
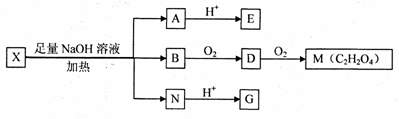 为推测X的分子结构,进行如下图的转化:
为推测X的分子结构,进行如下图的转化: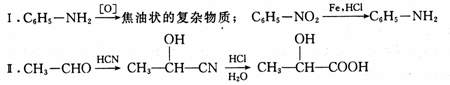
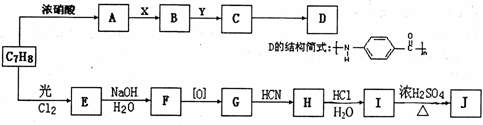
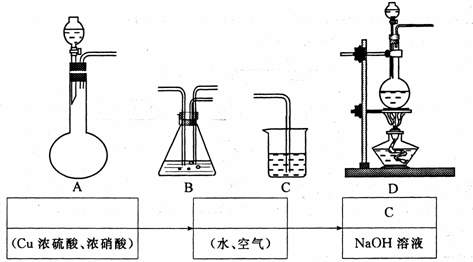 装置中选用适当的装置,并将它们的编号填入方框内
装置中选用适当的装置,并将它们的编号填入方框内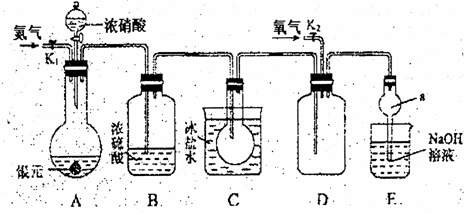
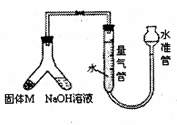 (2)合金样品固体M与氢氧化钠溶液反应的离子方程
(2)合金样品固体M与氢氧化钠溶液反应的离子方程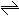 (11分)在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
(11分)在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据: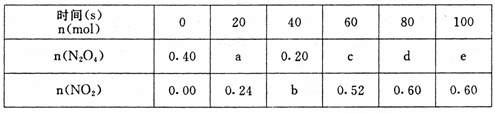
 C.使用高效催化剂 D.升高温度
C.使用高效催化剂 D.升高温度