22.
(08天津)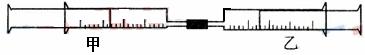
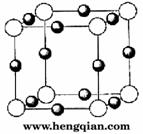
(A)如上图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题:
|
实验序号 |
甲针筒内物质 |
乙针筒内物质 |
甲针筒的现象 |
|
1 |
10mLFeSO4溶液 |
10mLNH3 |
生成白色沉淀,后变色 |
|
2 |
20mLH2S |
10mLSO2 |
|
|
3 |
30mLNO2(主要) |
10mLH2O(l) |
剩有无色气体,活 塞自动向内压缩 |
|
4 |
15molCl2 |
40mLNH3 |
|
⑴实验1中,沉淀最终变为 色,写出沉淀变色的化学方程式 。
⑵实验2甲针筒内的现象是:有 生成,活塞 移动(填向外、向内、不)。
反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入 溶液中。
⑶实验3中,甲中的30mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是
,写出NO2与H2O反应的化学方程式 。
 ⑷实验4中,已知:3Cl2+2NH3→N2+6HCl。甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为
,最后针筒中剩余气体的体积约为
mL。
⑷实验4中,已知:3Cl2+2NH3→N2+6HCl。甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为
,最后针筒中剩余气体的体积约为
mL。
16. (08广东)(12分)科学家一直致力研究常温、常压下“人工围氮”的新方法。曾有实验报道:在常温、常压、学照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压力1.0×105Pa、反应时间3 h):
|
T/K |
303 |
313 |
323 |
353 |
|
NH3生成量/(10-6mol) |
4.8 |
5.9 |
6.0 |
2.0 |
相应的热化学方程式如下: N2(g)+3H2O(1)=2NH3(g)+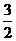 O2(g) ΔH=+765.2kJ·mol-1
O2(g) ΔH=+765.2kJ·mol-1
回答下列问题:
(1) 请在答题卡的坐标图中画出上述反应在有催化剂与无催化剂两种情况下反应过程
中体系能量变化示意图,并进行必要标注。
(2) 与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提
高其反应速率且增大NH3生成量的建议: 。
(3) 
 工业合成氨的反应为N2(g)+3H2(g)
? 2NH3(g)。设在容积为2.0L的密
工业合成氨的反应为N2(g)+3H2(g)
? 2NH3(g)。设在容积为2.0L的密
闭容器中充入0.60mol N2(g)和1.60 mol H2(g),.反应在一定条件下达到平衡时,NH3的物质的量分数(NH2的物质的量与反应体系中总的物质的量之比)为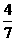 。计算
。计算
① 该条件下N2的平衡转化率
②  该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。
该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。
 ”“
”“ ”)。
”)。
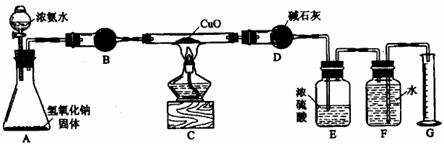
 21.( 08天津)(已知气体的摩尔质量越小,扩散速度越快。右图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的
21.( 08天津)(已知气体的摩尔质量越小,扩散速度越快。右图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的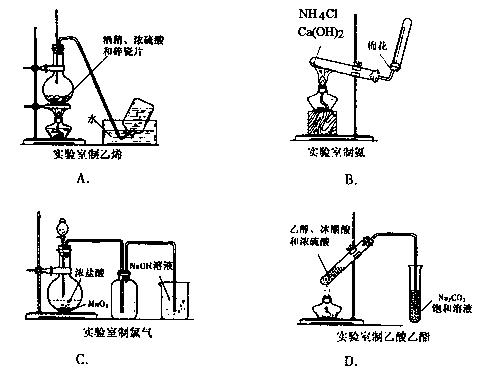
 Z+W
Z+W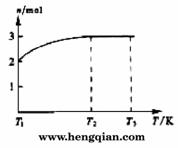 (4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。
(4)一定温度下,将1 mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。