21有一种多聚硼酸盐为无限网状结构,右图为
其结构单元示意图,其结构的基本单元可表示为
(B5On)m-,则m、n值分别是(D)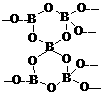
A、2,4 B、3,6 C、2,5 D、3,9
22下表数据是在某高温度下,金属镁和镍分别在氧气中进行氧化反应时,在金属表面生成氧化薄膜的实验记录:
|
反应时间 t/h |
1 |
4 |
9 |
16 |
25 |
|
MgO层厚Y/nm NiO层厚Y′/nm |
0.05a b |
0.20a 2b |
0.45a 3b |
0.80a 4b |
1.25a 5b |
*注:a和b均为与温度有关的常数 。请填空回答:
⑴金属高温氧化腐蚀速率可以用金属氧化膜的生长速率来表示,其理由是
反应速率可以用反应物的消耗速率,也可以用产物的生成速率。
⑵金属氧化膜的膜厚Y跟时间t所呈现的关系是(填直线、抛物线、对数或双曲线等类型):MgO氧化膜厚Y属直线 型,NiO氧化膜厚Y′属抛物线 型。
⑶Mg与Ni比较,哪一种金属具有良好的耐氧化腐蚀性:Ni ,其理由是:
它的腐蚀速率随时间的增长比镁的要慢。
23某学生为将含有少量杂质铜的氯化铁提纯.拟定以下实验步骤:
①把样品加蒸馏水溶解;②过滤除去杂质;③把滤液加热蒸干得到FeCl3晶体.
(1)你认为此方案是否科学,试用化学方程式和简要文字表达其理由.
答:
(1)不科学.加水后2FeCl3+Cu CuCl2+2FeCl2,过滤不能除去CuCl2;在 溶液蒸干过程中FeCl3+3H2O
CuCl2+2FeCl2,过滤不能除去CuCl2;在 溶液蒸干过程中FeCl3+3H2O Fe(OH)3+3HCl
Fe(OH)3+3HCl
(2)请你设计提纯氯化铁方案(只要求写出提纯步骤,最多只允许6步完成).
答:①加蒸馏水溶解;②加过量Fe粉;③过滤除去Cu和过量Fe;④通入适量氯气;⑤加入少 量盐酸; ⑥蒸发浓缩结晶得到FeCl3晶体.
24、由于用氯气对饮用水消毒,会使水中的有机物发生氯代,生成有机含氯化合物,于人体有害,世界环保联盟即将全面禁止这种消毒方法,建议采用广谱性具有强氧化性的高效消毒剂二氧化氯(ClO2)。ClO2极易爆炸,生产和使用时尽量用惰性气体稀释,避免光照、震动或加热。
(1)在ClO2分子中,所有原子是否都满足最外层8电子结构?否(填"是"或"否"),其中氯元素的化合价是+4;
(2)欧洲一些国家用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,且Cl2体积为ClO2的一半。表示这一反应的化学方程式是2NaClO3+4HCl=Cl2↑+2ClO2↑+2NaCl+2H2O
(3)我国广泛采用将经干燥空气稀释的氯气,通入填有固体亚氯酸钠(NaClO2)的柱内制得ClO2,表示这一反应的化学方程式是2NaClO2+Cl2=2ClO2+2NaCl,和欧洲的方法相比,我国这一方法的主要优点是生成的ClO2中不含Cl2杂质;
(4)在酸性溶液中,用草酸钠(Na2C2O4)还原NaClO3也可制得ClO2,表示这一反应的离子方程式是2ClO3-+C2O42-+4H+=2ClO2↑+2CO2↑+2H2O,此法的优点是析出的ClO2可被CO2稀释。
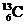 -NMR(核磁共振)可以用于含碳化合物的结构分析。
-NMR(核磁共振)可以用于含碳化合物的结构分析。 A.无机物
A.无机物 