21、(16分)实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:
请完成下列填空:
(1) 配制100mL 0.10mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后) →洗涤(并将洗涤液移入容量瓶)→ → →将配制好的溶液倒入试剂瓶中,贴上标签。
②称量0.4克氢氧化钠固体所需仪器有:天平(带砝码、镊子)、 、 。
(2) 取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
|
实验编号 |
NaOH溶液的浓度 (mol/L) |
滴定完成时,NaOH溶液滴入的体积(mL) |
待测盐酸溶液的体积 (mL) |
|
1 |
0.10 |
22.62 |
20.00 |
|
2 |
0.10 |
22.72 |
20.00 |
|
3 |
0.10 |
22.80 |
20.00 |
①滴定达到终点的标是 。
②根据上述数据,可计算出该盐酸的浓度约为 (保留两位有效数字)
③排去碱式滴定管中气泡的方法应采用操作 ,然后轻轻挤压玻璃球使尖嘴部分充满碱液。


甲 乙 丙
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 。(多选扣分)
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、称量前NaOH固体中混有Na2CO3固体
E、配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F、碱式滴定管尖嘴部分有气泡,滴定后消失
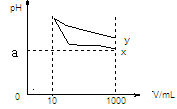 B、稀释后x溶液水电离的c(H+)比y溶液水电离的c(H+)大
B、稀释后x溶液水电离的c(H+)比y溶液水电离的c(H+)大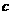 (NO
(NO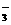 )>
)>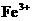 、
、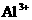 、
、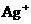 、
、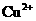 ,加入下列试剂,分别得到各含一种金属阳离子的沉淀.①通入
,加入下列试剂,分别得到各含一种金属阳离子的沉淀.①通入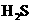 气体 ②通入
气体 ②通入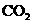 气体 ③加入盐酸 ④加入NaOH溶液.每次加入的试剂均过量且每次都把沉淀物滤出,其中实验操作的正确顺序是( B )
气体 ③加入盐酸 ④加入NaOH溶液.每次加入的试剂均过量且每次都把沉淀物滤出,其中实验操作的正确顺序是( B )