0 33752 33760 33766 33770 33776 33778 33782 33788 33790 33796 33802 33806 33808 33812 33818 33820 33826 33830 33832 33836 33838 33842 33844 33846 33847 33848 33850 33851 33852 33854 33856 33860 33862 33866 33868 33872 33878 33880 33886 33890 33892 33896 33902 33908 33910 33916 33920 33922 33928 33932 33938 33946 447348
 2C B.A+B
2C B.A+B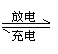 [例题5](05苏14) 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为
[例题5](05苏14) 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为  + 4H2O
+ 4H2O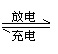 [反馈练习]镊铬(Ni--Cd)可充电电池在现代生活中有广泛应用。它的充放电过程按式进行:Cd(OH)2+2 Ni(OH)2
Cd+ NiO(OH)+2H2O。由此可知,该电池放电时的负极材料是
[反馈练习]镊铬(Ni--Cd)可充电电池在现代生活中有广泛应用。它的充放电过程按式进行:Cd(OH)2+2 Ni(OH)2
Cd+ NiO(OH)+2H2O。由此可知,该电池放电时的负极材料是
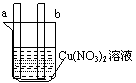
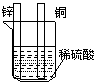
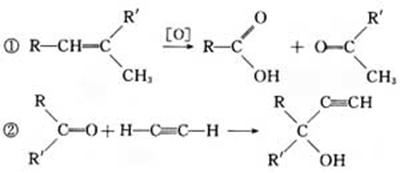

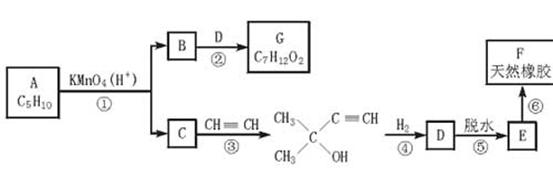
 G
;
G
;