9.(1)Na+ [ ∶Cl∶]¯ (2分) 2 H2(g)+ O2(g)= 2H2O(l);△H = -4a kJ/mol
‥
Cl2 + 2 OH¯ = Cl¯ + ClO¯ + H2O (3分) (3分)
(2) 三 ⅥA (各1分) 分子 (2分) 非极性 (2分)
∆
Cu + 2 H2SO4((浓) ==== CuSO4 + 2 SO2↑ + 2 H2O (3分)
|
(2) H2 + Cl2 = 2 HCl
(3) ∆
2 NH4Cl + Ca(OH)2 ==== 2 NH3↑ + 2 H2O + CaCl2 (每空各3分)
8.法国化学家伊夫·肖万获2005年诺贝尔化学奖。他发现了烯烃里的碳-碳双键会被拆散、重组,形成新分子,这种过程被命名为烯烃复分解反应 。烯烃复分解反应可形象地描述为交换舞伴。(如图所示)
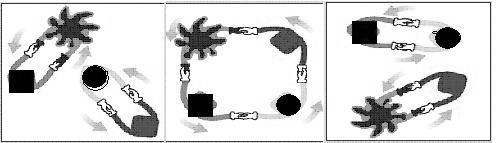
烯烃复分解反应中的催化剂是金属卡宾(如CH2==M),金属卡宾与烯烃分子相遇后,两
对舞伴会暂时组合起来,手拉手跳起四人舞蹈。随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴。后者会继续寻找下一个烯烃分子,再次“交换舞伴”。把C6H5CH2CH==CH2与CH2==M在一定条件下混合反应,下列产物不可能存在的是
A. C6H5CH2 CH2 C6H5 B. CH2= CH2
C. C6H5CH2CH==M D. C6H5CH2CH==CH CH2 C6H5
|
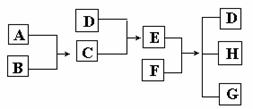
 ①A + B
M + D +
E; ② M +
E → A +
F + B
①A + B
M + D +
E; ② M +
E → A +
F + B
请针对以下两种不同情况回答:
(1)若A是一种钠盐,反应①是化学工业上制取单质E和化合物M的重要方法。则A的电子式为 ;已知单质D的气体在氧气中燃烧生成0.5 mol液态产物时,放出热量a kJ,反应的热化学方程式是_________________________;反应②的离子方程式为 。
(2)若A是一种含氧酸盐,可用于实验室中检验水的存在。1个A的酸根离子中共含有50个电子,其中含有一种元素X,X的原子最外层电子数是电子层数的2倍,则 X在元素周期表中的位置是第 周期 族。X单质的熔点是112.8℃ , 则X单质的晶体类型属于 晶体。X与碳单质在一定条件下可以生成CX2的化合物,其分子结构类似于CO2,则CX2属于(填“极性”或“非极性”) 分子。反应②的化学方程式为______________________________。
 (3)
(3)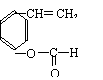
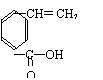 (4)
(4)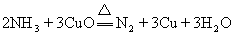
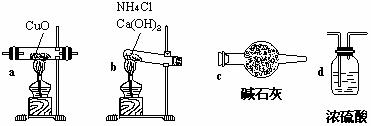 (1) 如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。
(1) 如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。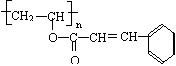 (15分)感光性高分子又称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料。其结构简式为:
(15分)感光性高分子又称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料。其结构简式为: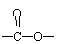
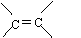 R的同分异构体有多种,其中含有苯环、
和
,且苯环上有两个对位取代基的结构简式是
R的同分异构体有多种,其中含有苯环、
和
,且苯环上有两个对位取代基的结构简式是