0 32652 32660 32666 32670 32676 32678 32682 32688 32690 32696 32702 32706 32708 32712 32718 32720 32726 32730 32732 32736 32738 32742 32744 32746 32747 32748 32750 32751 32752 32754 32756 32760 32762 32766 32768 32772 32778 32780 32786 32790 32792 32796 32802 32808 32810 32816 32820 32822 32828 32832 32838 32846 447348
 。当加入一种淡黄色粉末状固体物质时,有刺激性气味的混合气体放出,同时生成白色沉淀。当加入0.4mol淡黄色粉末时,共收集到0.3mol混合气体,且此时生成的沉淀量最多。此后继续加入淡黄色粉末时,沉淀量逐渐减少,当加入0.45mol粉末后,沉淀由0.3mol减少到0.2mol,再加入粉末后,沉淀就再减少。由实验现象及数据判断:
。当加入一种淡黄色粉末状固体物质时,有刺激性气味的混合气体放出,同时生成白色沉淀。当加入0.4mol淡黄色粉末时,共收集到0.3mol混合气体,且此时生成的沉淀量最多。此后继续加入淡黄色粉末时,沉淀量逐渐减少,当加入0.45mol粉末后,沉淀由0.3mol减少到0.2mol,再加入粉末后,沉淀就再减少。由实验现象及数据判断: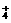 ;Fe2+、Cu2+
;Fe2+、Cu2+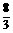 n(Fe)时,发生反应的化学方程式为______________________。
n(Fe)时,发生反应的化学方程式为______________________。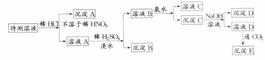 根据实验结果,回答下列问题:
根据实验结果,回答下列问题: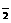 +CO2+3H2O=2Al(OH)3↓+CO
+CO2+3H2O=2Al(OH)3↓+CO