29.(13分)等电子体原理是指两个或两个以上的分子(或离子),它们的原子数相同,分子(或离子)中价电子数也相同,等电子体具有相似的电子结构、几何构型和性质。下表为部分元素等电子体的分类、空间构型表。
|
等电子体类型 |
代表物质 |
空间构型 |
|
四原子24电子等电子体 |
SO3 |
平面三角型 |
四原子26电子 等电子体 等电子体 |
SO32- |
三角锥型 |
|
五原子32电子等电子体 |
CCl4 |
四面体型 |
|
六原子40电子等电子体 |
PCl5 |
三角双锥型 |
|
七原子48电子等电子体 |
SF6 |
八面体型 |
请回答下列问题:
(1)指出下列物质离子、分子的空间构型:
BrO3- ,CO32- ,HClO4 ;
(2)由第一、二周期元素组成,与F2互为等电子体的离子是 (写一种),有机分子是 、 (写两种);
(3)双原子14电子的等电子体共同特点是物质中都具有共价叁键,请举出相应的3个例子
(分子或离子),每个分子或离子中含 个σ键, 个π键;
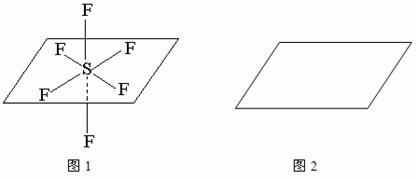
(4)SF6的空间结构如图1所示,请按照图1表示方法,在图2中表示OSF4分子中O、S、F原子的空间位置。已知OSF4分子中O、S间为共价双键,S、F间为共价单键。
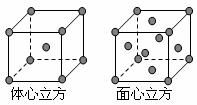
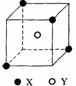 (1)晶体中每个Y同时吸引着 个X,每个X同时吸引 着个Y,该晶体化学式为 ;
(1)晶体中每个Y同时吸引着 个X,每个X同时吸引 着个Y,该晶体化学式为 ;