23、(12分)某学生用0.1000mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A、用蒸馏水洗干净滴定管
B、用待测定的溶液润洗酸式滴定管
C、用酸式滴定管取稀盐酸 20.00mL,注入锥形瓶中,加入酚酞。
D、另取锥形瓶,再重复操作一次
E、检查滴定管是否漏水
F、取下碱式滴定管用标准的KOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2-3cm处,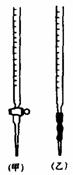 再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
G、把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)
(2)操作F中应该选择右图中哪根滴定管(填标号)
(3)滴定终点溶液颜色的变化是
(4)滴定结果如下表所示:
|
滴定次数 |
待测溶液体积/ml |
标准溶液的体积/ml |
|
|
滴定前刻度 |
滴定后刻度 |
||
|
1 |
20 |
1.02 |
21.03 |
|
2 |
20 |
2.00 |
25.00 |
|
3 |
20 |
0.60 |
20.6 |
滴定中误差较大的是第_______次实验,造成这种误差的可能原因是____________________________。
A.碱式滴定管在装液前未用标准KOH溶液润洗2-3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.达到滴定终点时,仰视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(5)则该盐酸的浓度为 mol/lL
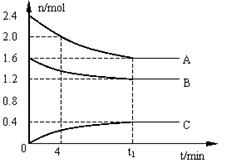 C浓度变化如图所示。(1)写出该反应的方程式:
C浓度变化如图所示。(1)写出该反应的方程式:
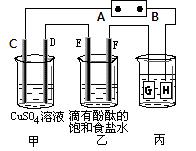 原因是(用离子方程式表示)
。
原因是(用离子方程式表示)
。 2Q(g)+nR(g)。反应达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应方程式中的n值为( )
2Q(g)+nR(g)。反应达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应方程式中的n值为( )  2SO3(g) △H=-197 kJ·mol-1,在相同温度下向一密
2SO3(g) △H=-197 kJ·mol-1,在相同温度下向一密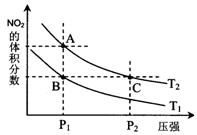 反应N2O4(g)
反应N2O4(g) 2NO2(g) △H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g) △H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )