网址:http://m.1010jiajiao.com/timu3_id_325853[举报]
碳族元素是形成化合物种类最多的元素。
(1)碳原子2个2p电子的运动状态不相同的方面是_______;C5HxN分子中C、N原于最外层都达到8电子稳定结构,则x的值可能为_______ (选填序号)。
a.10 b.11 c.13 d.15
(2)如图是金刚石晶体的结构示意图。则关于金刚石的描述正确的是 (选填序号)。
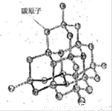
a.C-C键键角都为109°28’ b.最小的环由6个C原子构成
c.可溶于非极性溶剂 d.l mol金刚石含有4 mol C-C键
(3)以下比较错误的是________(选填序号)。
a.稳定性SiH4>CH4 b.沸点SiH4>CH4
c.熔点SiC>Si d.键能C=C>C-C
(4)NaBH4是广泛使用的有机反应还原剂,其中H为-1价,SiO2为其制备原料之一。
①配平以下制备NaBH4的化学方程式:□Na2B4O7+□Na+□SiO2+□H2→□NaBH4+□Na2SiO3
②反应中被还原的元素为________。
(5)碳酸钙是石灰石、方解石等的主要成分,可以形成“喀斯特”地貌、钟乳和石笋,有关反应的化学方程式为_________________________________________。
(6)若物质组成相似,可相互推算组成元素的相对原子质量。某学习小组模拟求算锗的相对原子质量,测得了锗酸钠中Na和Ge的质量分数、硅酸钠中Na和Si的质量分数,他们还需查阅的数据是______(选填序号)。
a.氧元素的相对原子质量
b.硅元素的相对原子质量
c.钠元素的相对原子质量
查看习题详情和答案>>
(15分)
由碳、氢、氧三种元素组成的某有机物X的相对分子质量为136,其中碳、氢元素的质量分数之和为76.5﹪.又知X中含有甲基,苯环上的一氯代物有两种。X经热的酸性KMnO4溶液处理后转化为Y,1mol Y与足量NaHCO3溶液反应生成标准状态下44.8L CO2气体。
据此完成下列要求。
(1)X中含氧官能团的名称为 ,1mol Y最多可与 mol Na反应。
(2)已知A、B、C、D均与X互为同分异构体,且均是有一个取代基的芳香族化合物,其中B可以发生银镜反应。相关转化关系如下图。
①A的结构简式为 。A~K的各有机物中,属于酸的是 (填字母)。
②C与足量的NaOH溶液加热时发生反应的化学方程式为: ,该反应中涉及到的有机反应类型为 。
③属于芳香族化合物的E的同分异构体有 种(不含E)。
④足量的G与Y在一定条件下发生反应的化学方程式为: 。
(15分)
由碳、氢、氧三种元素组成的某有机物X的相对分子质量为136,其中碳、氢元素的质量分数之和为76.5﹪.又知X中含有甲基,苯环上的一氯代物有两种。X经热的酸性KMnO4溶液处理后转化为Y,1mol Y与足量NaHCO3溶液反应生成标准状态下44.8L CO2气体。
据此完成下列要求。
(1)X中含氧官能团的名称为 ,1mol Y最多可与 mol Na反应。
(2)已知A、B、C、D均与X互为同分异构体,且均是有一个取代基的芳香族化合物,其中B可以发生银镜反应。相关转化关系如下图。

①A的结构简式为 。A~K的各有机物中,属于酸的是 (填字母)。
②C与足量的NaOH溶液加热时发生反应的化学方程式为: ,该反应中涉及到的有机反应类型为 。
③属于芳香族化合物的E的同分异构体有 种(不含E)。
④足量的G与Y在一定条件下发生反应的化学方程式为: 。
查看习题详情和答案>>
由碳、氢、氧三种元素组成的某有机物X的相对分子质量为136,其中碳、氢元素的质量分数之和为76.5﹪.又知X中含有甲基,苯环上的一氯代物有两种。X经热的酸性KMnO4溶液处理后转化为Y,1mol Y与足量NaHCO3溶液反应生成标准状态下44.8L CO2气体。
据此完成下列要求。
(1)X中含氧官能团的名称为 ,1mol Y最多可与 mol Na反应。
(2)已知A、B、C、D均与X互为同分异构体,且均是有一个取代基的芳香族化合物,其中B可以发生银镜反应。相关转化关系如下图。

①A的结构简式为 。A~K的各有机物中,属于酸的是 (填字母)。
②C与足量的NaOH溶液加热时发生反应的化学方程式为: ,该反应中涉及到的有机反应类型为 。
③属于芳香族化合物的E的同分异构体有 种(不含E)。
④足量的G与Y在一定条件下发生反应的化学方程式为: 。
查看习题详情和答案>>由碳、氢、氧三种元素组成的某有机物X的相对分子质量为136,其中碳、氢元素的质量分数之和为76.5﹪.又知X中含有甲基,苯环上的一氯代物有两种。X经热的酸性KMnO4溶液处理后转化为Y,1mol Y与足量NaHCO3溶液反应生成标准状态下44.8L CO2气体。
据此完成下列要求。
(1)X中含氧官能团的名称为 ,1mol Y最多可与 mol Na反应。
(2)已知A、B、C、D均与X互为同分异构体,且均是有一个取代基的芳香族化合物,其中B可以发生银镜反应。相关转化关系如下图。
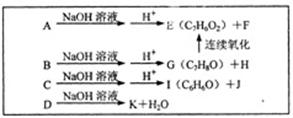
①A的结构简式为 。A~K的各有机物中,属于酸的是 (填字母)。
②C与足量的NaOH溶液加热时发生反应的化学方程式为: ,该反应中涉及到的有机反应类型为 。
③属于芳香族化合物的E的同分异构体有 种(不含E)。
④足量的G与Y在一定条件下发生反应的化学方程式为: 。