2.在763K、3.04×104kPa时,用CO和H2作为原料合成CH3OH,存在下列平衡:
CO(气)+2H2(气)⇌CH3OH(气)
当原料中H2和CO的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响。
(1)设H2和CO的起始物质的量之比为m,平衡时CO的转化率为a,平衡混合物中甲醇的体积分数为y,试推断m、a、y,三者的相互关系并以y=f(d,m)的函数表达式表示出来。
答案: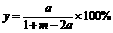
(2)将下表已知数据代人导出的表达式中进行计算,把计算结果填人表中有关空格中:
|
m |
a |
Y |
|
1 |
0.25 |
|
|
2 |
0.45 |
|
|
3 |
|
19.35% |
答案:
|
m |
a |
y |
|
1 |
0.25 |
16.67% |
|
2 |
0.45 |
21.43% |
|
3 |
0.56 |
19.35% |
(3)根据上表数据,判断用CO和H2合成甲醇时,H2和CO的最佳体积比是多少?并简述依据。
答案:分析上表中数据不难看出,当,m=2时,CO的转化率较大,此时平衡混合气中CH3OH的体积分数最高
 最佳比为H2:CO=2:1
最佳比为H2:CO=2:1

 2SO3(正反应为放热反应)
2SO3(正反应为放热反应) Ag2O(固)+SO3(气)
Ag2O(固)+SO3(气)