(五)铁:
1. 物理性质:银白色(有时黑色)、固体、质软
物理性质:银白色(有时黑色)、固体、质软
2.化学性质:
⑴铁与氧气
 ⑵铁与酸:Fe+ HCl=
⑵铁与酸:Fe+ HCl=
Fe+H2SO4=
⑶铁与硫酸铜:Fe+CuSO4=
3.铁的合金:生铁与钢
|
|
纯铁 |
钢 |
生铁 |
|
组成(含碳量) |
0 |
0.03-2% |
2%-4.3% |
小   大 大 |
|||
|
性能 |
硬 度 |
小   大 大 |
|
|
韧 性 |
好   差 差 |
练习:
1.长期存放石灰水的试剂瓶内壁上常附着一层白膜,其名称是 ,形成过程的化学方程式是 ;要除去这层白膜,可向瓶中加少量_______(填名称)溶解,反应的化学方程式是 。
2.要检验生石灰中是否含有石灰石,可加入少量 (填名称),如果有 产生(填现象),就说明生石灰中含有石灰石;要除去生石灰中的石灰石,可将其 ,反应的化学方程式是 。
3.
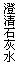
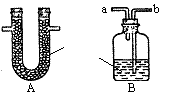 右图,为了除去氢气中的少量水蒸气和二氧化碳,可
右图,为了除去氢气中的少量水蒸气和二氧化碳,可
将混合气体先通过 ,再通过 ,(填A、B)
即得到纯净、干燥的氢气;当混合气体通过B时,气体应
从 通入(填a、b)。
4.为了测定水煤气的组成,用右图A、B、C装置连接后,
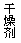
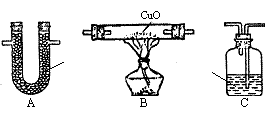 将水煤气通入。测定时发现A中质量增加,B中黑色粉末
将水煤气通入。测定时发现A中质量增加,B中黑色粉末
变红,C中出现浑浊。回答:
⑴装置连接顺序应是:(填A、B、C)
水煤气→ → → ;
⑵A质量增加,说明水煤气中含有 ;
⑶C中的现象说明水煤气中含有 。
5.写出除去下列物质中的少量杂质(括号内为杂质)时所发生反应的化学方程式:
⑴ CO中混有少量CO2: ;
⑵ FeSO4(CuSO4): ;
⑶ NaCl(Na2CO3): ;
⑷ Fe粉(Fe2O3): 。
(三)具有可燃性和还原性的三种物质:氢气、一氧化碳、碳
1.物理性质:
|
|
颜色 |
气味 |
状态 |
密度 |
溶解性 |
|
H2 |
无色 |
无味 |
气体 |
比空气 |
溶于水 |
|
CO |
无色 |
无味 |
气体 |
比空气 |
溶于水 |
|
C |
金刚石和石墨的物理性质不同,是因为它们中的
不同。 金刚石和石墨是由 元素组成的 的物质;它们的物理性质 ,但化学性质 。(填:相同、不同) |
2.化学性质:
|
H2 |
可燃性 |
⑵还原性 |
|
H2+ O2 点燃 |
H2+ CuO △ |
|
|
CO |
CO+ O2
点燃 |
CO+ CuO △ |
|
C |
C+ O2 点燃 |
C+ CuO 高温 |
(二)具有可燃性的三种气体:氢气、一氧化碳、甲烷
1.物理性质:
|
|
颜色 |
气味 |
状态 |
密度 |
溶解性 |
|
H2 |
无色 |
无味 |
气体 |
比空气 |
溶于水 |
|
CO |
无色 |
无味 |
气体 |
比空气 |
溶于水 |
|
CH4 |
无色 |
无味 |
气体 |
比空气 |
溶于水 |
2.化学性质(可燃性):
|
H2 |
可燃性 |
H2、CO、CH4的检验 |
|
H2+ O2 点燃 |
点燃后,⑴在火焰上方罩一干冷的小烧杯,烧杯内壁没有 ,该气体是 ;⑵在火焰上方罩一内壁附有澄清石灰水的小烧杯,石灰水变 ,该气体是
;另一气体就是 。 |
|
|
CO |
CO+ O2
点燃 |
|
|
CH4 |
CH4+ O2 点燃 |
(一)三大气体的性质和用途:氧气、氢气、二氧化碳
1、氢气、氧气、二氧化碳性质的比较:
1)物理性质:
|
三大气体 |
颜色 |
气味 |
状态 |
密度 |
溶解性 |
|
H2 |
无色 |
无味 |
气体 |
比空气 |
溶于水 |
|
O2 |
无色 |
无味 |
气体 |
比空气 |
溶于水 |
|
CO2 |
无色 |
无味 |
气体 |
比空气 |
溶于水 |
2)化学性质:
|
H2 |
⑴可燃性 |
⑵还原性 |
||
|
H2+ O2 点燃 |
H2+ CuO △ |
|||
|
O2 |
⑴与金属 |
⑵与非金属 |
⑶与化合物 |
|
|
Mg+ O2 点燃 Fe+ O2 点燃 |
C+ O2 点燃 S+ O2 点燃 P+ O2 点燃 |
CH4+ O2 点燃 C2H5OH+ O2 点燃 CO+ O2 点燃 |
||
|
CO2 |
⑴与水 |
⑵与石灰水 |
⑶与碳 |
|
|
CO2+ H2O
= |
CO2+ Ca(OH)2
= |
CO2+ C 高温 |
||
2、氧气、氢气、二氧化碳用途的比较:
|
氢气用途 |
氧气用途 |
二氧化碳用途 |
|
⑴填充气球 ⑵高能燃料 ⑶冶炼重要金属 |
⑴支持燃烧 ⑵供给呼吸 ⑶用于炼钢 |
⑴灭火 ⑵作工业原料(制饮料、纯碱、化肥等) ⑶“干冰”用于人工降雨 ⑷植物的光合作用 |


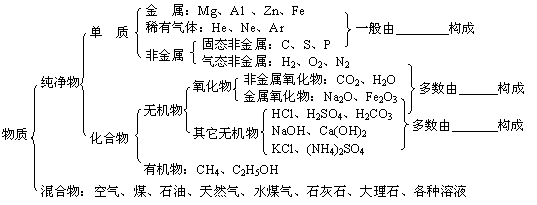 (三)物质的分类
(三)物质的分类
 A水是由氢、氧元素组成的;B水是由水分子构成的;C一个水分子是由两个氢原子和一个氧原子构成的;D水分子是氢、氧元素组成的;E水是由两个氢原子和一个氧原子构成的。
A水是由氢、氧元素组成的;B水是由水分子构成的;C一个水分子是由两个氢原子和一个氧原子构成的;D水分子是氢、氧元素组成的;E水是由两个氢原子和一个氧原子构成的。
