33.(7分)某化学兴趣小组对水蒸气通过灼热的焦炭后,得到的混合气体主要成分产生了兴趣。同学们决定通过实验进行探究。
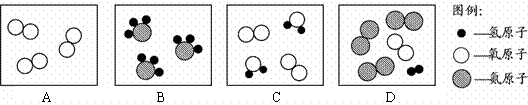
[提出猜想]该混合气体主要成分为一氧化碳、二氧化碳、氢气和水蒸气。
[查阅资料]a.无水硫酸铜遇水由白色变为蓝色。
b.碱石灰是固体氢氧化钠和氧化钙的混合物。
c.氢气、一氧化碳均能在加热的条件下与氧化铜反 应。
应。
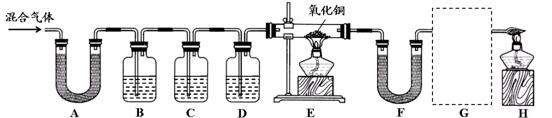 [实验过程]同学们在老师的指导下设计了如下图所示装置,并进行了实验(部分夹持仪器已略去)。
[实验过程]同学们在老师的指导下设计了如下图所示装置,并进行了实验(部分夹持仪器已略去)。
(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊。由此得出的结论为 。写出装置B中反应的化学方程式 。
(2)装置C和D中的药品分别为 。
(3)同学们通过观察装置E、F中的现象后,证明了混合气中含有氢气。为了证明第四种气体的存在,装置G中的药品、现象和结论是 。
[实验结论]猜想正确。
[实验反思]
经过讨论,同学们将上图中装置C~H进行了简化,改进后的装置如下图所示。
 (3)干燥管中碱石灰的作用为
。
(3)干燥管中碱石灰的作用为
。
|
|
实验操作 |
实验现象 |
实验结论 |
|
① |
在尖嘴处点燃气体, 。 |
。 |
。 |
|
② |
。 |
。 |
。 |
(4)同学们为了验证通过干燥管后气体的成分,继续进行的实验为:
30. (7分)下列字母表示的各种物质是初中化学常见的不同物质。其中A、B、C、D存在如图所示的转化关系(其中“→”表示可以进行转化),四种物质中均含有两种相同的元素。
(7分)下列字母表示的各种物质是初中化学常见的不同物质。其中A、B、C、D存在如图所示的转化关系(其中“→”表示可以进行转化),四种物质中均含有两种相同的元素。
(1)B是纯碱,其化学式为 。
(2)X是由三种元素组成的酸,请写出X与B反应生成D、Y和Z的化学方程式 。
(3)A在受热时可以分解生成B、Y和Z,那么A的化学式为 。
(4)向A的溶液中加入C的溶液,可以生成B和Z,请写出该化学方程式 。
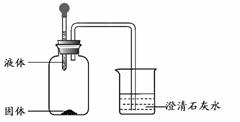
(5)从上述物质中选2种为一组,按下图所示装置进行实验。将胶头滴管中的液体滴入瓶中,看到烧杯中的澄清石灰水变浑浊。写出符合要求的两组物质。
|
物质 序号 |
液体 |
固体 |
|
① |
|
|
|
② |
|
|
(6)请根据以上七种物质分析,下列说法正确的是 。
a.X与A、B、C反应均有气泡冒出 b.七种物质中A、B、D属于盐类
c.Y与C反应可以生成B和Z d.X、Y、Z的相对分子质量依次减小

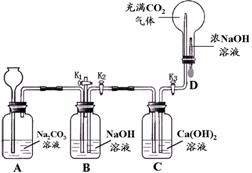 (1)先打开K1,关闭K2和K3,从长颈漏斗
(1)先打开K1,关闭K2和K3,从长颈漏斗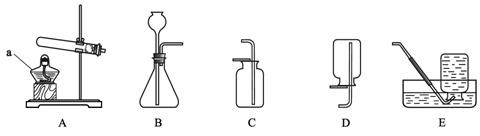
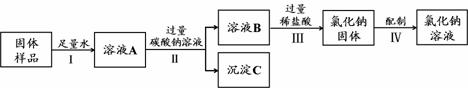
 性。
性。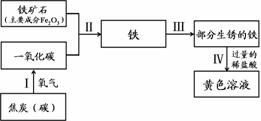 (2)根据右侧转化关系图,回答问题。
(2)根据右侧转化关系图,回答问题。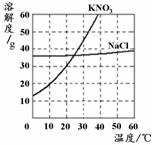
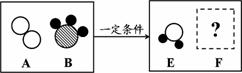
 中生成的E和F的质量比 。
中生成的E和F的质量比 。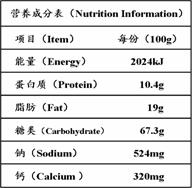 (1)这种饼干
(填“能”或“不能”)提
(1)这种饼干
(填“能”或“不能”)提 所需六种营养素,其中所含的钠、钙是
所需六种营养素,其中所含的钠、钙是