13.(2010北京中考,40) 在研讨酸、碱、盐相互间反应关系时,甲、乙两组同学利用碳酸钠溶液按照以下步骤完成实验(假设每步反应都完全)。
第一步:向碳酸钠溶液中加试剂X,过滤,得白色沉淀;
第二步:向该沉淀中加试剂Y,沉淀全部溶解,生成气体,得无色溶液;
第三步:向该溶液中加试剂Z,过滤,最终得不溶于酸的白色沉淀和硝酸镁溶液。
(1)甲、乙两组同学共进行三次实验,其中所选的试剂均不相同,乙组同学最终得到的不溶于酸的白色沉淀不同于甲组。请将化学式填入下表:
|
|
试剂X |
试剂Y |
试剂Z |
最终得到的白色沉淀 |
|
|
甲组 |
① |
MgCl2 |
|
|
AgCl |
|
乙组 |
② |
|
HNO3 |
|
|
|
③ |
|
|
|
(2)请写出乙组两次实验中碳酸钠溶液与试剂X反应的化学方程式:__________________,_________________________。
解析:由题干信息可知第二步向该沉淀中加试剂Y一定是酸,第三步得到的不溶于酸的白色沉淀是AgCl或?BaSO4,那么甲最终得到的白色沉淀是AgCl,则试剂Y是HCl,因另一种生成物是硝酸镁溶液,所以试剂Z是AgNO3;乙组同学最终得到的不溶于酸的白色沉淀不同于甲组那就是BaSO4,实验②第一步得到的白色沉淀是BaCO3,所以试剂X是BaCl2或Ba(OH)2,试剂Z是MgSO4;实验③是另一种酸则是硫酸,所以试剂X是Mg(NO3)2,试剂Z是Ba(NO3)2。
答案:(1)
|
|
试剂X |
试剂Y |
试剂Z |
最终得到的白色沉淀 |
|
|
甲组 |
① |
|
HCl |
AgNO3 |
|
|
乙组 |
② |
BaCl2(或Ba(OH)2) |
|
MgSO4 |
BaSO4 |
|
③ |
Mg(NO3)2 |
H2SO4 |
Ba(NO3)2 |
(2)BaCl2+Na2CO3====BaCO3↓+2NaCl(或Ba(OH)2+Na2CO3====BaCO3↓+2NaOH)
Mg(NO3)2+Na2CO3====MgCO3↓+2NaNO3
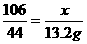 则x=31.8 g
则x=31.8 g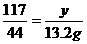 则y=35.1 g
则y=35.1 g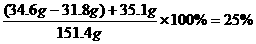 。
。