0 23746 23754 23760 23764 23770 23772 23776 23782 23784 23790 23796 23800 23802 23806 23812 23814 23820 23824 23826 23830 23832 23836 23838 23840 23841 23842 23844 23845 23846 23848 23850 23854 23856 23860 23862 23866 23872 23874 23880 23884 23886 23890 23896 23902 23904 23910 23914 23916 23922 23926 23932 23940 447348
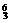 Li B.
Li B.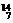 N
C.
N
C.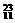 Na
D.
Na
D.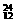 Mg E.
Mg E.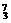 Li F.
Li F.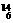 C G.C60 H .CH3CH2COOH I.HO-CH2CH2-CHO J.金刚石 K. P4 L.SiO2 M.NH4Cl
C G.C60 H .CH3CH2COOH I.HO-CH2CH2-CHO J.金刚石 K. P4 L.SiO2 M.NH4Cl 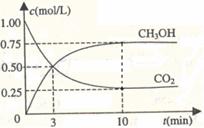 CO2(g)+3H2(g)
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H= - 49.0kJ·mol-1测得CO2和CH3OH(g)的浓度随时间变化如上图所示。
CH3OH(g)+H2O(g) △H= - 49.0kJ·mol-1测得CO2和CH3OH(g)的浓度随时间变化如上图所示。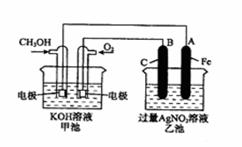
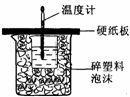 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: AsO33-+I2+H2O
AsO33-+I2+H2O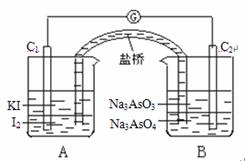 试回答下列问题:
试回答下列问题: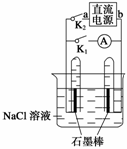 右图是某同学设计的验证原电池和电解池的实验装置,下列有关说法不正确的是( )
右图是某同学设计的验证原电池和电解池的实验装置,下列有关说法不正确的是( ) Cd(OH)2 + 2Ni(OH)2 有关该电池的说法正确的是( )
Cd(OH)2 + 2Ni(OH)2 有关该电池的说法正确的是( )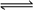 PCl3(g)+Cl2(g) ①
PCl3(g)+Cl2(g) ①