21.(12分)某学习小组利用铁与稀硫酸的反应,进行“探究影响化学反应速率因素”的实验。结果如下表:
|
实验 序号 |
铁的质量/g |
铁的 形态 |
V(H2SO4) /mL |
c(H2SO4) /mol·L-1 |
反应前溶液 的温度/℃ |
金属完全消 失的时间/s |
|
1 |
0.10 |
片状 |
50 |
0.8 |
20 |
200 |
|
2 |
0.10 |
粉状 |
50 |
0.8 |
20 |
25 |
|
3 |
0.10 |
片状 |
50 |
1.0 |
20 |
125 |
|
4 |
0.10 |
片状 |
50 |
1.0 |
35 |
50 |
请分析上表信息,回答下列问题。
(1)实验1、2 表明 对反应速率有影响,其规律是 。
(2)仅表明反应物浓度对反应速率产生影响的实验有 (填实验序号)。
(3)该探究实验中,影响反应速率的因素还有 ,体现该影响因素的实验有 (填实验序号)。
(4)进行实验3时,若将稀硫酸 改为50 mL 2.0 mol·L-1 盐酸(其他条件不变),发现:放出气泡的速率,盐酸明显比硫酸快。你认为可能的原因是 。
(忽略温度对反应速率的影响)
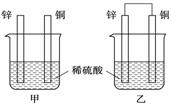 19.(6分)将锌片和铜片以下图所示两种方式分别插入同浓度稀硫酸中。
19.(6分)将锌片和铜片以下图所示两种方式分别插入同浓度稀硫酸中。
(1)以下叙述中,正确的是 (填标号)。
A.装置甲、乙中铜片表面均无气泡产生
B.装置甲、乙中稀硫酸的浓度均减小
C.装置乙中锌片是正极,铜片是负极
D.装置乙中产生气泡的速率比装置甲快
(2)装置乙中,总反应的离子方程式为 ;若导线上通过0.2 mol电子,消耗锌的质量为 g。
20.(16分)现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
T |
M层上有6个电子 |
|
X |
最外层电子数是次外层电子数的2倍 |
|
Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性[来源:. |
|
Z |
元素最高正价是+7价 |
(1)元素T为 元素(填元素名称)。元素X的一种核素可测定文物年代,这种核素的符号是 。
(2)元素Y在周期表中的位置 。
(3)元素Z的原子结构示意图为 。
(4)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),能证明这一事实的依据是 。
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是 (填酸的化学式),理由是 。
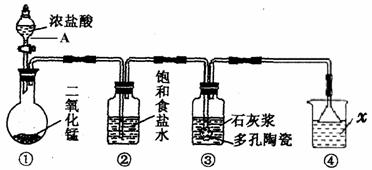 (12分) 下图是一个制取氯气并以氯气为原料进行某些反应的装置。(夹持和加热装置省略)。
(12分) 下图是一个制取氯气并以氯气为原料进行某些反应的装置。(夹持和加热装置省略)。 “华安、连城、永安、漳平一中、龙海二中、泉港一中”四地六校联考
“华安、连城、永安、漳平一中、龙海二中、泉港一中”四地六校联考 2010-2011学年下学期第二次月考
2010-2011学年下学期第二次月考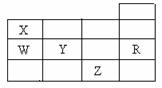 右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是