0 23335 23343 23349 23353 23359 23361 23365 23371 23373 23379 23385 23389 23391 23395 23401 23403 23409 23413 23415 23419 23421 23425 23427 23429 23430 23431 23433 23434 23435 23437 23439 23443 23445 23449 23451 23455 23461 23463 23469 23473 23475 23479 23485 23491 23493 23499 23503 23505 23511 23515 23521 23529 447348

 :
______________________________________。
:
______________________________________。
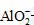 +2H2O
+2H2O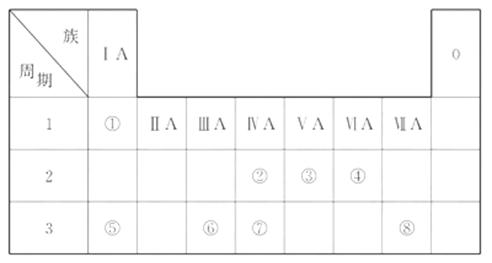

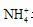 水解, 故要使其浓度与Cl-
相等, 则要补充NH3·H2O。
水解, 故要使其浓度与Cl-
相等, 则要补充NH3·H2O。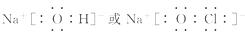
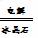 4Al+3O2↑
4Al+3O2↑ 反应H2+I2 ==== 2HI, 形成2 mol HI放出2×299 kJ的热量, 所以生成1 mol HI时放出热量为
反应H2+I2 ==== 2HI, 形成2 mol HI放出2×299 kJ的热量, 所以生成1 mol HI时放出热量为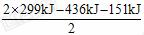 =5.5
kJ。
=5.5
kJ。 速率是______, N2的转化率是___________________________________________,
H2的转化率是_________________。
速率是______, N2的转化率是___________________________________________,
H2的转化率是_________________。
 ____________________。
____________________。 位置。(1)氢原子核外只有1个电子, 与碱金属元素原子最外层电子数相同, 氢元素在绝大多数化合物中显+1价, 与碱金属元素在化合物中显+1价相似, 所以, 现行元素周期表将氢排在第ⅠA族, 所以, 碱金属位于第ⅠA族, 但不能说位于第ⅠA族的元素都是碱金属。(2)在金属氢化物中, 钠、钾、钙元素都显正化合价, 所以氢元素显-1价, 与金属卤化物中卤族元素化合价相同, 所以, 氢元素也可以排在第ⅦA族。
位置。(1)氢原子核外只有1个电子, 与碱金属元素原子最外层电子数相同, 氢元素在绝大多数化合物中显+1价, 与碱金属元素在化合物中显+1价相似, 所以, 现行元素周期表将氢排在第ⅠA族, 所以, 碱金属位于第ⅠA族, 但不能说位于第ⅠA族的元素都是碱金属。(2)在金属氢化物中, 钠、钾、钙元素都显正化合价, 所以氢元素显-1价, 与金属卤化物中卤族元素化合价相同, 所以, 氢元素也可以排在第ⅦA族。 2SO3,
在混合气体中充
2SO3,
在混合气体中充 O2、O2和SO3中
O2、O2和SO3中