典例3:制备卤磷酸钙荧光粉所用的高纯氯化钙中混有氯化镁杂质,除去的方法是把氯化钙的水溶液加热到90-95℃,在不断搅拌下加入适当的沉淀剂,使镁生成沉淀过滤除去。此沉淀剂最好选用
A.氢氧化钙乳浆 B.碳酸钠溶液 C.碳酸氢钠溶液 D.氢氧化钠溶液
研析:碳酸氢钠溶液不能除去氯化镁杂质;碳酸钠溶液可以与氯化钙溶液反应生成碳酸钙沉淀;氢氧化钠溶液虽然能较好的除去氯化镁杂质,但同时引入了杂质钠离子,并且有部分氯化钙可与其反应生成微溶物氢氧化钙而损失。
答案:A。
方法导引:除杂方法有物理方法和化学方法。除杂的原则为不增(在除去杂质时不能引入新的杂质)、不减(要保留物质不损失)、易分(反应的生成物易分离)。
|
拓展 变式 3.下列广告语在科学性上没有错误的是 A.这种矿泉水绝对纯净,不含任何离子 B.这种饮料中不含任何化学物质 C.这种口服液含有丰富的氮、磷、锌等微量元素 D.没有水就没有生命 3.研析:矿泉水中一般含有Ca2+、Mg2+等多种离子,饮料中的水及其它营养成分都属于“化学物质”,氮、磷都是常量元素,A、B、C、错误。D正确。此题与人们的饮食保健密切相关,该学生以亲切感、新鲜感,解决此类题需要学生灵活运用所学知识,而不是靠死记硬背,这样有助于克服传统教学囿于传授书本知识的偏向,避免了“题海”带来的思维僵化,有助于学生懂得周围的科技环境,适应日益技术话的日常生活,应付不断进步的科技革新,有能力对科学技术、人类生存相关的社会问题发表意见并作出决策。 答案:D。 |
典例2:在科学史上,中国有许多重大的发明和发现,为现代物质文明奠定了基础。以下发明或发现属于化学史上中国对世界做出重大贡献的是
① 造纸 ② 印刷技术 ③ 火药 ④ 指南针 ⑤ 炼铜、炼铁、炼钢 ⑥ 合成有机高分子材料 ⑦ 人工合成牛胰岛素 ⑧ 提出原子--分子学说
A.①②③④⑧ B.①③⑤⑦ C.②④⑥ D.⑤⑥⑦⑧
研析:造纸、印刷技术、火药、指南针、炼铜、炼铁、炼钢、人工合成牛胰岛素等都属于中国重大的发明和发现,对世界科学的发展做出了贡献。但印刷技术、指南针与化学关联不大。
答案:B。
启发引申:化学是一门具有创造性的、实用的科学。可以说,化学创造了“一个崭新的自然界”。化学发展到现在,我们的衣、食、住、行都离不开化学。在化学发展史上,中国有许多发明和发现,比如远在春秋战国时期,我们就掌握炼铁的技术了。中国为化学的发展做出了突出的贡献,相信在当前乃至将来的化学发展中,必然会做出更大的贡献。
|
拓展 变式 2.与近代化学的诞生无关的是 A.化学元素的概念 B.英国化学家、物理学家波义耳 C.著名物理学家爱因斯坦 D.古代的化学实践活动 2.研析:任何事物是相互联系的,现代化学的产生离不开古代的化学实践活动;1661年,在前人工作的基础上,英国化学家、物理学家波义耳提出化学元素的概念,标志着近代化学的诞生。而爱因斯坦是上一世纪的人物,他出生时,近代化学已诞生两个世纪了。 答案:C。 |
▲ 综合思维探究
典例1:古诗词是古人为我们留下的宝贵精神财富。下列诗句中只涉及物理变化的是
A.野火烧不尽,春风吹又生 B.春蚕到死丝方尽,蜡炬成灰泪始干
C.只要功夫深,铁杵磨成针 D.爆竹声中一岁除,春风送暖人屠苏
研析:因化学变化与物理变化的本质区别是变化后是否有新物质生成。A中的“野火烧不尽”、B中的“蜡炬成灰泪始干”都牵扯到物质的燃烧,都有“CO2”这种新物质生成;D中的“爆竹声中一岁除”牵扯到火药的爆炸,当然也有新物质生成;只有C中的“铁杵磨成针”只是物质由粗到细,由大到小的过程,没有新物质生成,属于物理变化。
答案:C。
总结提升:本题考查的知识点比较明确,即物理变化与化学变化的区别。难度较小,但题目非常新颖,联系大家熟悉的古诗词,不仅扩大了知识面,更会体会到确实是“化学无处不在,我们的生活离不开化学”。这就无形中增加了同学们学化学、用化学的兴趣。
|
拓展 变式 1.下列变化不属于化学变化的是 A.溶洞的形成过程 B.物质的燃烧 C.合成高分子材料 D.矿石的粉碎 1.研析:在溶洞的形成过程中,CaCO3变为Ca(HCO3)2,部分Ca(HCO3)2随水流走,部分Ca(HCO3)2又变为CaCO3,形成了石笋、石柱和钟乳石,是化学变化。物质的燃烧,一般是物质跟空气中的氧气发生的反应,有新的物质生成,属于化学变化。合成高分子材料属人工合成新物质,也是化学变化。矿石的粉碎过程中无新物质生成,属物理变化,不是化学变化。 答案:D。 |
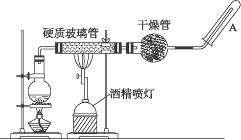
 Fe3O4+4H2↑
Fe H2O
Fe3O4+4H2↑
Fe H2O