27.(10分)某学生小组用HNO3与大理石反应来探究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为250mL、大理石用量为11.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
|
编号 |
T/K |
大理石规格 |
HNO3浓度/mol·L-1 |
实验目的 |
|
① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响。 |
|
② |
298 |
|
|
|
|
③ |
308 |
|
|
|
|
④ |
298 |
|
|
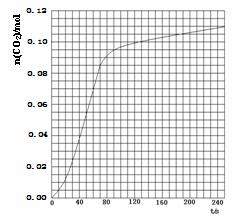 (2)实验①中CO2的物质的量随时间变化的关系见图:
(2)实验①中CO2的物质的量随时间变化的关系见图:
计算在70-90 s范围内HNO3的平均反应速率_____________________
(忽略溶液体积变化)。
26.为提纯下列物质(括号内为少量杂质),所选用的除杂式试剂和分离方法正确的是
|
|
提纯物质 |
除杂试剂 |
分离法 |
|
A |
KCl溶液(FeCl3) |
氨水 |
过滤 |
|
B |
乙酸乙酯(乙酸) |
乙醇和浓硫酸 |
分液 |
|
C |
Fe粉(Al粉) |
NaOH溶液 |
过滤 |
|
D |
乙醇(H2O) |
金属钠 |
蒸馏 |
第Ⅱ卷(非选择题,共42分)
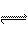 (6分)恒温下,将amolN2与bmolH2的混合气体通入一个固定的密闭容器中。发生如下反应:
(6分)恒温下,将amolN2与bmolH2的混合气体通入一个固定的密闭容器中。发生如下反应: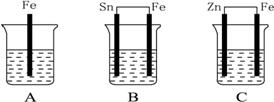
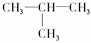 与CH3-CH2-CH2-CH3
与CH3-CH2-CH2-CH3