0.05 mol 0.05 mol 高☆考♂资♀源?网 0.05mol 0.05mol
M(H2)=0.1g (3分)
选做题:答案:(10分)
(1)(1分)
|
(3)(2分)a b (4)(3分)224mL
高☆考♂资♀源?网
28、(6分) 在盛有500mL0.1 mol·L-1CuSO4和0.4 mol·L-1H2SO4混合溶液的大烧杯中。用锌、铜作电极,用导线连接形成原电池,当电极锌消耗6.5g时,试完成:
(1)写出电极反应式:
负极__________________ ;
正极_______________________________ 。
(2)计算产生氢气的质量。
高☆考♂资♀源?网
选做题:(10分)某短周期元素A,其最高价氧化物对应水化物甲与其气态氢化物乙反应可生成盐丙。已知乙的密度是同温同压下H2密度的8.5倍。请回答:
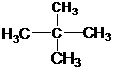
(1)A单质的电子式为 。
(2)甲具有不稳定性,其发生分解的化学反应方程式为
。
实验室保存甲的方法是 。
(3)在一定条件下,将乙放入固定容积的密闭容器中使其发生分解反应,已知
△H>0,达到平衡状态后,改变其中一个条件X,Y随X的变化符合图中曲线的
是
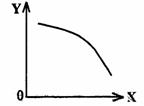 (选填字母)
(选填字母)
a.当X表示温度时,Y表示乙的物质的量
b.当X表示压强时,Y表示乙的转化率
c.当X表示反应时间时,Y表示混合气体
|
d.当X表示乙的物质的量时,Y表示某一生成物
的物质的量
(4)现有硫酸和甲的混合液20mL,其中硫酸的物质的量浓度为2mol·L-1,甲的
物质的量浓度为1mol·L-1。向该混合液中加入0.96g铜粉,假设只生成一种无色
气体,则所收集到的气体的体积在标准状况下为 。
高☆考♂资♀源?网

(2)Cu2+ + Zn == Zn2+ + Cu; 2H+ + Zn == Zn2+ + H2↑
26、(8分)某课外兴趣小组对H2O2的分解速率做了如下实验探究。
⑴下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2制取150mL O2所需的时间(秒)
|
反应条件 /浓度 |
30% H2O2 |
15% H2O2 |
10% H2O2 |
5% H2O2 |
|
无催化剂、不加热 |
几乎不反应 |
几乎不反应 |
几乎不反应 |
几乎不反应 |
|
无催化剂、加热 |
360 |
480 |
540 |
720 |
|
MnO2催化剂、加热 |
10高☆考♂资♀源?网 |
25高☆考♂资♀源?网 |
60 |
120 |
①该研究小组在设计方案时, 考虑了浓度、 、 等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响? 。
⑵将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试。测定结果如下:
|
催化剂(MnO2)高☆考♂资♀源?网 |
操作情况高☆考♂资♀源?网 |
观察结果高☆考♂资♀源?网 |
反应完成所 需的时间 |
|
粉末状 |
混合不振荡 |
剧烈反应,带火星的木条复燃 |
3.5分钟高☆考♂资♀源?网 |
|
块状 |
反应较慢,火星红亮但木条未复燃 |
30分钟 |
①写出H2O2发生的化学反应方程式___________ _________。
②实验结果说明催化剂作用的大小与______ ____________ 有关。

 和
和 
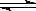 2NO(g) + O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是高☆考♂资♀源?网
2NO(g) + O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是高☆考♂资♀源?网