摘要: 在盛有500mL0.1 mol·L-1CuSO4和0.4 mol·L-1H2SO4混合溶液的大烧杯中.用锌.铜作电极.用导线连接形成原电池.当电极锌消耗6.5g时.试完成: (1)写出电极反应式: 负极 , 正极 . (2)计算产生氢气的质量. 高☆考♂资♀源?网 选做题:某短周期元素A.其最高价氧化物对应水化物甲与其气态氢化物乙反应可生成盐丙.已知乙的密度是同温同压下H2密度的8.5倍.请回答: (1)A单质的电子式为 . (2)甲具有不稳定性.其发生分解的化学反应方程式为 . 实验室保存甲的方法是 . (3)在一定条件下.将乙放入固定容积的密闭容器中使其发生分解反应.已知 △H>0.达到平衡状态后.改变其中一个条件X.Y随X的变化符合图中曲线的 是 a.当X表示温度时.Y表示乙的物质的量 b.当X表示压强时.Y表示乙的转化率 c.当X表示反应时间时.Y表示混合气体 2,4,6 的密度 d.当X表示乙的物质的量时.Y表示某一生成物 的物质的量 (4)现有硫酸和甲的混合液20mL.其中硫酸的物质的量浓度为2mol·L-1.甲的 物质的量浓度为1mol·L-1.向该混合液中加入0.96g铜粉.假设只生成一种无色 气体.则所收集到的气体的体积在标准状况下为 . 高☆考♂资♀源?网 (2)Cu2+ + Zn == Zn2+ + Cu, 2H+ + Zn == Zn2+ + H2↑
网址:http://m.1010jiajiao.com/timu3_id_216449[举报]
(9分) 在盛有500mL0.1mol/LCuSO4和0.4mol/LH2SO4混合溶液的大烧杯中。用锌、铜作电极,用导线连接形成原电池,当电极锌消耗6.5g时,试完成:
(1)写出电极反应式:负极__________________ ;正极_______________________________。
(2)电极上共析出氢气的质量为 克。
查看习题详情和答案>>把在空气中久置的铝片 5.0 g投入盛有500mL0.5mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如右的坐标曲线来表示,下列推论错误的是
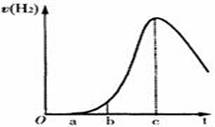
A.t由0→a段不产生氢气是因为表面的氧化物隔离了铝和硫 酸溶液
B.t由b→c段产生氢气的速率增加较快的主要原因之一是温度升高
C.t=c时反应处平衡状态
D.t>c产生氢气的速率降低主要是因为溶液中c(H+)降低
查看习题详情和答案>>
如图1所示三个烧瓶中分别装入含酚酞的0.01mol?L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质.

(1)含酚酞的0.01mol?L-1 CH3COONa溶液显浅红色的原因为:
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01mol?L-1 CH3COONa溶液中加入少量浓盐酸,则CH3COO-水解平衡移动的方向为_
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO- )-c(Na+)=
(5)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图2,则HX的酸性
查看习题详情和答案>>

(1)含酚酞的0.01mol?L-1 CH3COONa溶液显浅红色的原因为:
CH3COO-+H2O?CH3COOH+OH-
CH3COO-+H2O?CH3COOH+OH-
(用离子方程式表示).(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是
B、D
B、D
.A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01mol?L-1 CH3COONa溶液中加入少量浓盐酸,则CH3COO-水解平衡移动的方向为_
右
右
_; 加入NaOH固体,则CH3COO-水解平衡移动的方向为左
左
(填“左”、“右”或“不移动”)(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO- )-c(Na+)=
9.9×10-7mol/L
9.9×10-7mol/L
.(填准确数值)(5)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图2,则HX的酸性
>
>
(填“>”、“=”或“<”)醋酸的酸性;稀释后,HX溶液中水电离出来的c(H+)>
>
醋酸溶液水电离出来c(H+)(填“>”、“=”或“<”).现有等体积混合而成的四组气体:①NO2+NO ②NO2+O2 ③NH3+N2 ④NO+N2,将盛有各组混合气体的试管倒立在盛有足量水的水槽中,试管内页面上升的高度分别为h1、h2、h3、h4,其中关系正确的是( )
| A、h2>h3>h1>h4 | B、h3>h2>h1>h4 | C、h1=h2=h3=h4 | D、h1>h2>h3>h4 |
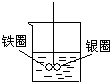 如图在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入硫酸铜溶液.一段时间后可观察到的现象是( )
如图在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入硫酸铜溶液.一段时间后可观察到的现象是( )