19. 某学生在研究性学习的课程中选定的课题是:测定能使带 火星木条复燃的氧气体积分数的最小值。实验步骤如下:
某学生在研究性学习的课程中选定的课题是:测定能使带 火星木条复燃的氧气体积分数的最小值。实验步骤如下:
①取5---6只集气瓶,用量筒装水分别测定它们的容积并标记:
②向集气瓶中分别装入其总容积的10%、20%、30%、40%、50%的水,并用毛玻璃盖住,依次编号为l、2、3、4、5;
③向大试管中加入1:10(质量比)的Mn02和KCl03的混合物,加热使其反应,分别用排水集气法将上述1-5号瓶中水排去:
④将带火星的木条依次插入1-5号瓶中,观察并记录现象,列入下表:
|
集气瓶号 |
1 |
2 |
3 |
4 |
5 |
|
木条火星的状况 |
微亮 |
亮 |
很亮 |
复燃 |
复燃 |
请回答下列问题:
(1)用排水集气法收得氧气后,3号瓶中氧气的体积分数约为:
(2)如果要得到更精确的数据,下一步实验研究应如何做?
(3)从已取得的实验数据分析,用“使带火星的木条是否复燃”的方法来检验集气瓶中是否充满氧气的方法是否可靠?
。
 a.弱氧化性:与硫化氢反应:
a.弱氧化性:与硫化氢反应:
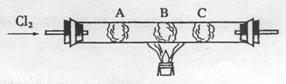

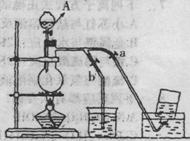 (3)烧瓶中发生反应的离子方程式是 ▲ 烧杯中发生反应的离子方程式是 ▲
(3)烧瓶中发生反应的离子方程式是 ▲ 烧杯中发生反应的离子方程式是 ▲  a、
.b、
a、
.b、