0 19298 19306 19312 19316 19322 19324 19328 19334 19336 19342 19348 19352 19354 19358 19364 19366 19372 19376 19378 19382 19384 19388 19390 19392 19393 19394 19396 19397 19398 19400 19402 19406 19408 19412 19414 19418 19424 19426 19432 19436 19438 19442 19448 19454 19456 19462 19466 19468 19474 19478 19484 19492 447348

 金属元素的化合物,依据下列各物质间转化关系,判断各物质的化学式
金属元素的化合物,依据下列各物质间转化关系,判断各物质的化学式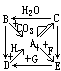 A_______ B_________ C_________ D_______
A_______ B_________ C_________ D_______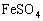 滴入NaoH浓溶液立刻得到白色
滴入NaoH浓溶液立刻得到白色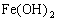 沉淀,随这,白色沉淀在空气中被氧化,颜化加深,变绿
沉淀,随这,白色沉淀在空气中被氧化,颜化加深,变绿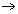 墨绿
墨绿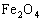 组成可以写成FeO
组成可以写成FeO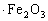 ,写成盐的形式为
,写成盐的形式为
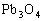 写成两种氧化物的式子为______写成盐的形式为___________
写成两种氧化物的式子为______写成盐的形式为___________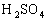 反应,混合物放热,当反应体系不再显强酸性时,他将反应停止.
反应,混合物放热,当反应体系不再显强酸性时,他将反应停止.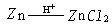 (2)
(2)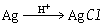 (3)
(3)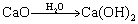
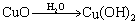 (5)
(5) 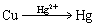 (6)
(6)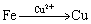
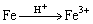 (8)
(8)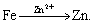 (9)
(9)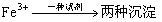

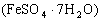 加强热,流出一种油状液体,放出刺激味气体(
加强热,流出一种油状液体,放出刺激味气体(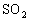 )反应器中固体变为红色,试写出这一分解反应的化学反应方程式.
)反应器中固体变为红色,试写出这一分解反应的化学反应方程式.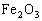 ,可用稀盐酸.稀硫酸除去.Fe与稀
,可用稀盐酸.稀硫酸除去.Fe与稀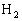 ,Fe与
,Fe与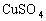 溶液反应,本身溶解置换出Cu;Fe和冷浓
溶液反应,本身溶解置换出Cu;Fe和冷浓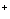 )
)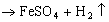 ,
,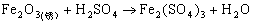 反应,观察到:锈先溶解,溶液由无色变黄,(
反应,观察到:锈先溶解,溶液由无色变黄,(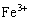 为棕黄色),继而有气体产生,直至铁片全消失.引起反应前后质量变化的是跑走的H
为棕黄色),继而有气体产生,直至铁片全消失.引起反应前后质量变化的是跑走的H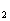 .用
.用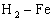 关系找到没生锈的Fe则生锈部分为
关系找到没生锈的Fe则生锈部分为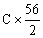 溶液中含
溶液中含
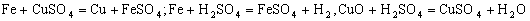
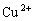 了,含有的阳离子为
了,含有的阳离子为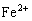 固体中一定有铜.
固体中一定有铜. 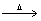 乙+B ②A+D
乙+B ②A+D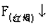 为F,对热不稳定分解为,
为F,对热不稳定分解为,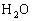 顺序推出.
顺序推出.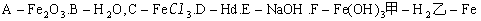
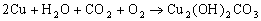

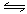 氧化物
氧化物 氢氧化物的转化关系的知识
氢氧化物的转化关系的知识