23.(18分)(1)地壳中某主要元素是现代许多高科技产品的重要组成元素之一,足见化学对现代物质文明起作重要的推动作用。请根据你的所见所闻填写以下空白:
①光导纤维的主要成分 (填写化学式)
②目前应用最多的太阳能电池的光电转化材料是 (填写名称)
③神奇无比的集成电路芯片的主要成分 (填写名称)
④用作吸附剂、催化剂的载体的人造分子筛大多是一类为 (填写名称)
⑤写出工业上以某矿物为原料制备该元素的高纯度单质的化学方程式
(2)下列五个图中,横坐标表示加入的物质的量,纵坐标表示生成沉淀的量从A-E中选择各题要求的序号填入表中
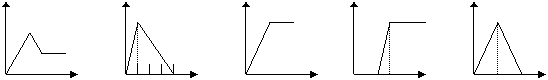
A B C D E
|
溶液 |
加入的物质 |
答案序号 |
|
MgCl2
和AlCl3的混和液 |
滴加NaOH至过量 |
|
|
NaAlO2溶液 |
滴加稀HCl至过量 |
|
|
含少量NaOH的NaAlO2溶液 |
通过量的CO2 |
|
|
AlCl3溶液 |
通过量的NH3 |
|
|
饱和石灰水 |
通CO2至过量 |
|
(3)类比思维是化学研究中常用的思维方法,它能帮助研究人员从一个问题出发来巧妙地解决一类本质相似的问题。已知:过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如:Na2O2+CO=Na2CO3 2Na2O2+2CO2=2Na2CO3+O2 。
试回答下列问题:
①写出Na2O2分别与SO2、SO3反应的化学方程式:
。
。
②请你总结归纳出过氧化钠与常见气态非金属氧化物发生反应的规律:
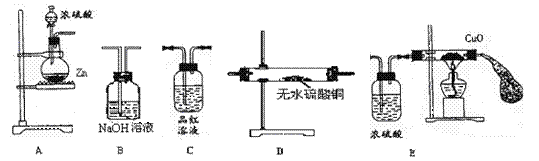 (1)这些装置连接的正确顺序是(填A.B.C.D.E):
(1)这些装置连接的正确顺序是(填A.B.C.D.E):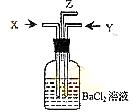 (3)已知二氧化硫能被稀硝酸氧化。现将碳跟浓硫酸共热产生
(3)已知二氧化硫能被稀硝酸氧化。现将碳跟浓硫酸共热产生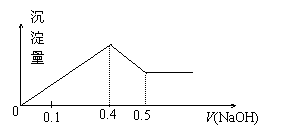 现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为 ( )
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为 ( )