1、填表(以11号-18号元素为例元素性质的变化规律)
|
元素 |
11Na |
12Mg |
13A1 |
14Si |
15P |
16S |
17C1 |
18Ar |
||
|
(1)电子排布 |
电子层数相同,最外层电子数从1依次递增到8 |
|||||||||
|
(1)原子半径, |
 原子半径(递减) 原子半径(递减) |
不可 |
||||||||
|
|
比 |
|||||||||
|
(3)主要化合价 |
十1 |
十2 |
+3 |
十4 -4 |
十5 -3 |
+6 -2 |
+7 -1 |
|
||
|
(4)金属性、非金属性 |
 金属性(减弱),非金属性(增强) 金属性(减弱),非金属性(增强) |
|||||||||
|
(5)单质与水或酸反 应置换氢难易 |
与水剧烈反应 |
与水加热缓慢反应 |
与酸反应,但速率比镁慢 |
______ |
__ |
|||||
|
(6)氢化物化学式 |
______ |
SiH4 |
PH3 |
H2S |
HCl |
__ |
||||
|
(7)与H2化合的难易 程度 |
______ |
 由( 难 )到( 易 ) 由( 难 )到( 易 ) |
|
__ |
||||||
 |
||||||||||
|
(8)氢化物稳定性 |
______ |
 稳定性(增大) 稳定性(增大) |
__ |
|||||||
|
(9)最高价氧化物化 学式 |
Na20 |
MgO |
Al2O3 |
SiO2 |
P205 |
S03 |
C1207 |
__ |
||
|
最高价 |
(10)化学式 |
NaOH |
Mg(OH)2 |
Mg(OH)2 |
H4Si04 |
H4Si04 |
H2S04 |
HCl04 |
__ |
|
|
氧化物 |
(11)酸碱性 |
强碱 |
中强碱 |
两性氢氧化物 |
弱酸 |
中强酸 |
强酸 |
最强酸(同周期) |
__ |
|
|
对应水 化物 |
(12)变化 规律 |
 碱性(减弱),酸性(增强) 碱性(减弱),酸性(增强) |
__ |
|||||||
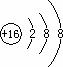 。
。  ,E与B形成的化合物H∶....∶H或H∶....∶....∶H,A、B、E形成的化合物Na+[∶....∶H ]-,D与E形成的化合物
,E与B形成的化合物H∶....∶H或H∶....∶....∶H,A、B、E形成的化合物Na+[∶....∶H ]-,D与E形成的化合物