0 16091 16099 16105 16109 16115 16117 16121 16127 16129 16135 16141 16145 16147 16151 16157 16159 16165 16169 16171 16175 16177 16181 16183 16185 16186 16187 16189 16190 16191 16193 16195 16199 16201 16205 16207 16211 16217 16219 16225 16229 16231 16235 16241 16247 16249 16255 16259 16261 16267 16271 16277 16285 447348
 CO2↑ + 4NO2↑ + 2H2O
CO2↑ + 4NO2↑ + 2H2O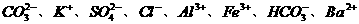 八种离子,请按要求填写:
八种离子,请按要求填写: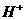 大量共存的有_________。
大量共存的有_________。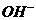 大量共存的有_________。
大量共存的有_________。
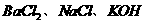 三种溶液区别开,此试剂是( )
三种溶液区别开,此试剂是( )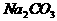 B.
盐酸 C.
硫酸 D.
B.
盐酸 C.
硫酸 D.
 溶液
溶液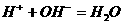 的离子方程式表示下列化学反应的是( )
的离子方程式表示下列化学反应的是( ) 溶液和盐酸反应 B.
溶液和盐酸反应 B.
 和硫酸反应
和硫酸反应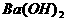 和醋酸反应 D.
和醋酸反应 D.
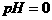 的无色透明溶液中,能大量共存的离子组是( )
的无色透明溶液中,能大量共存的离子组是( )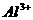 、
、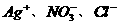 B.
B.
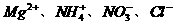
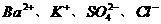 D.
D.