30.(5分)某学生在课外活动中用一定量的二价金属R和稀硫酸反应来制取氢气,所做5次实验结果记录如下表(假设每次实验所产生的氢气全部被收集,体积在同温同压下测定)。
|
实验编号 |
R 的质量/克 |
稀硫酸的体积/毫升 |
生成H2的体积/升 |
|
1 |
1.5 |
50.0 |
1.47 |
|
2 |
2.0 |
50.0 |
1.96 |
|
3 |
2.2 |
50.0 |
2.16 |
|
4 |
2.5 |
50.0 |
2.16 |
|
5 |
3.0 |
50.0 |
2.16 |
根据上述实验结果进行分析、计算,并回答下列问题:
(1)上述实验中,金属一定过量的组的编号是 ,稀硫酸一定过量的组的编号是 。
(2)若在当时实验条件下,H2的密度为0.085克/升,则反应所用金属R的相对原子质量为 。
(3)若所使用的稀硫酸密度为1.12克/厘米3,则反应所用的硫酸溶液中溶质的质量分数为 。
|
食 品名 称 |
500g食品的味精 含量/mg |
|
春 卷 |
400 |
|
排 骨 |
240 |
|
水 饺 |
130 |
29.(3分)酒楼的食品在制作时常加入味精,味精是一种有机化合物一谷氨酸钠,其化学式为C5H8NO4Na。右表为某酒楼常见食品中味精的含量,根据题中的信息计算:(列式计算)
⑴ 谷氨酸钠的相对分子质量为 ;其中碳、氢元素的质量比为 ;
⑵ 若某同学一次吃了200g春卷,他食用了 mg味精,其中含钠元素的质量为 mg(结果保留一位小数)。
27.(6分)某化学科技活动小组的同学学过氨气后,查阅资料发现氨气一种密度比空气小、且极易溶于水的气体,在常温下遇到HCl气体,会产生大量白烟,白烟的主要成分是这两种气体化合形成的铵盐M的固体小颗粒。带着极大的兴趣,小组的同学想先制取干燥的氨气,然后利用它来探究与HCl气体的反应。经过小组讨论,他们设计了如下的实验装置:
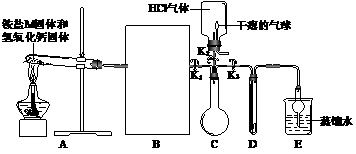

图1 图2
注:整套装置的气密性良好(且图1中的B和C装置还不完善,有待于同学们在实验过程中选择和补充),D装置的试管内有一张湿润的红色石蕊试纸;E装置的作用是吸收反应产生的剩余氨气,防止其进入空气,造成污染;碱石灰固体是氢氧化钠固体和生石灰固体的混合物。
(1)请你参与小组的探究:
|
实验目的 |
实验操作及现象 |
|
制取一烧瓶干燥的氨气 |
①按图1装配仪器和试剂,其中图1方框内的B装置应选择图2中的______(填序号);请在C装置的烧瓶内画出连接止水夹K1和K3的导管长度情况。 ②打开止水夹K1和K3,关闭止水夹K2,点燃酒精灯加热,当出现__________________________现象时,停止加热,并关闭止水夹K1和K3。 |
|
探究氨气与HCl气体的反应 |
③打开止水夹K2,一段时间后,除了看到有大量白烟生成这一现象外,还可观察到______________________________,导致这一现象的主要原因是_________。 |
(2)氯化氢气体与氨气发生化合反应,生成一种铵盐,写出反应的化学方程式:
21. (8分)请你结合下列装置图和题中信息回答问题:
(8分)请你结合下列装置图和题中信息回答问题:


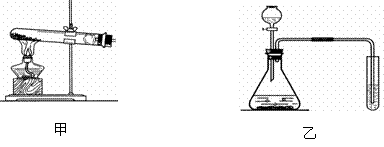
(1)实验室用甲装置制氧气的化学方程式是______________________________ 。反应完全后冷却,往试管中加入足量的水,搅拌、过滤,得到黑色粉末。该黑色粉末与过氧化氢接触有大量气泡产生,反应的化学方程式是____________________________________。
(2)某化学兴趣小组用乙装置制取并检验二氧化碳。实验过程中,可观察到试管里产生____________色沉淀,反应的化学方程式是________________________ 。产生沉淀后继续通入二氧化碳,过一段时间后,发现沉淀溶解变成澄清溶液。为了确定沉淀溶解成澄清溶液的原因,该小组的同学进行了相关探究。
[ 提出问题 ] 沉淀为什么能溶解变成澄清溶液?
[ 查阅资料 ] 碳酸钙溶于酸,碳酸氢钙[Ca(HCO3)2]溶于水。
[ 猜想与假设 ] ①溶液呈酸性;②反应生成了碳酸氢钙。
[ 实验与结论 ]
|
实验操作 |
实验现象 |
实验结论 |
|
实验Ⅰ:
|
测得被测液的pH=8 |
猜想①______________。 (填“成立”或“不成立”) |
|
实验Ⅱ:取沉淀溶解后的澄清溶液于另一支试管中,加入______________________。 |
有气体产生 |
反应的化学方程式为: _____________________________。 猜想②成立。 |
通过探究得知,生成的沉淀会与二氧化碳、水反应生成了可溶于水的碳酸氢钙。
 ⑶生成白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是
。
⑶生成白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是
。
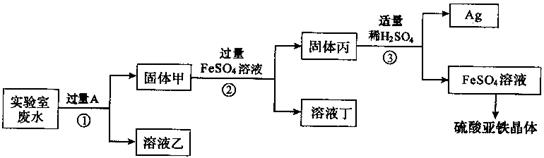 AgNO3、Zn(NO3)2、Fe(NO3)2,该校实验小组拟从该废水中回收银,并得到副产品硫酸亚铁晶体。实验方案如下所示(实验过程中未引入其它的金属元素)
AgNO3、Zn(NO3)2、Fe(NO3)2,该校实验小组拟从该废水中回收银,并得到副产品硫酸亚铁晶体。实验方案如下所示(实验过程中未引入其它的金属元素) ⑴下列铁制品中,制造铁丝利用了铁的性质是______________。
⑴下列铁制品中,制造铁丝利用了铁的性质是______________。