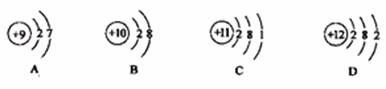
24.[参考答案]答案:(1)Ⅱ(2)硫酸钠和硫酸(或Na2SO4 和H2SO4)
(2)
|
实验操作 |
实验现象 |
实验结论 |
|
方案一:取少许反应后的 溶液置于试管中,向其中加入_碳酸钠(或氧化铁) |
产生气泡(或红褐色固体逐渐溶解,溶液由无色变为黄色) |
小亮的观点正确 |
|
方案二:取少许反应后的 溶液置于试管中,向其中加入__锌(或石蕊溶液) |
产生气泡(或溶液显红色) |
(3)①氢离子和氢氧根离子反应生成了水分子
②反应前的锌原子和铜离子变成了锌离子和铜原子
③有新分子或新原子或新离子生成(或产生新粒子)(2分)
[思维点拨]以实验探究的形势考查酸碱盐的知识,是近几年就为常见的典型题目。根据已知条件,有题目可知所探究的主题是“酸和碱的溶液能发生反应吗?”。由于发生反应:2NaOH+H2SO4==Na2SO4+2H2O,无色酚酞溶液由红色变为无色,只能确定NaOH已反应完全,不能确定H2SO4是否过量,因此反应后的溶质除了有Na2SO4,还有可能有H2SO4,如果小亮的观点正确,就是说存在H2SO4,而检验H2SO4的方法有很多:如用碳酸钠、金属锌、石蕊等。第(3)问从微观角度分析反应实质:硫酸中存在自由移动的H+、SO42-、NaOH溶液中存在自由移动的Na+、OH-,反应后的溶液中仍然含有SO42- Na+,而H+、OH-不存在,说明反应中H+、OH-结合成H2O分子,通过分析揭示了化学反应的微观本质是有新的分子等粒子产生。
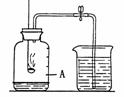 4-2图是某同学设计的验证氧气约占空气总体积1/5的实验装置图。下列操作过程对实验结果的影响说法正确的是( )
4-2图是某同学设计的验证氧气约占空气总体积1/5的实验装置图。下列操作过程对实验结果的影响说法正确的是( )