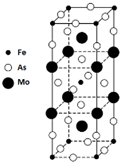
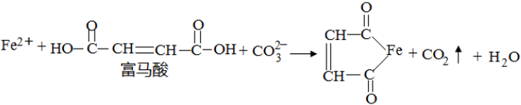2.“神州八号”飞船成功发射升空之后,完成了与1个月前发射的“天宫一号”的成功交会对接,其中新材料铝锂合金为“太空之吻”提供了保障.下列关于铝锂合金的认识正确的( )
| A. | 铝锂合金是铝与锂形成的一种化合物 | |
| B. | 锂是碱金属元素,性质活泼,铝锂合金与水反应生成氢气 | |
| C. | 铝离子和锂离子的核外电子排布相同 | |
| D. | 若铝锂合金中锂含量为1.1%,则127.3g铝锂合金中含有锂原子0.2mol |
15.现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤 形,A与氢元素形成化合物AH5除了配位键外还有离子键和极性键.
(2)某同学根据上述信息,所画的C电子排布图如图违背了泡利 原理.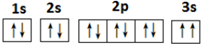
(3)DE3 中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形.检验F元素的方法是焰色反应.
(4)A2与B22+互为等电子体,B22+的电子式可表示为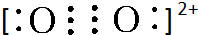 ;1mol B22+中含有的π键数目为2NA.
;1mol B22+中含有的π键数目为2NA.
(5)下列电子云图象均为成键后电子云图象,其中可表示一个E原子与一个E原子的是E,表示一个氢原子与一个E原子的是D.

0 172460 172468 172474 172478 172484 172486 172490 172496 172498 172504 172510 172514 172516 172520 172526 172528 172534 172538 172540 172544 172546 172550 172552 172554 172555 172556 172558 172559 172560 172562 172564 172568 172570 172574 172576 172580 172586 172588 172594 172598 172600 172604 172610 172616 172618 172624 172628 172630 172636 172640 172646 172654 203614
| A.元素原子的核外p电子总数比s电子总数少1 |
| B.元素价电子排布式为nsnnp2n |
| C.元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| D.原子核外所有p轨道全满或半满 |
| E.元素的主族序数与周期数的差为4 |
| F.是前四周期中电负性最小的元素 |
(2)某同学根据上述信息,所画的C电子排布图如图违背了泡利 原理.

(3)DE3 中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形.检验F元素的方法是焰色反应.
(4)A2与B22+互为等电子体,B22+的电子式可表示为
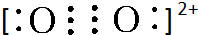 ;1mol B22+中含有的π键数目为2NA.
;1mol B22+中含有的π键数目为2NA.(5)下列电子云图象均为成键后电子云图象,其中可表示一个E原子与一个E原子的是E,表示一个氢原子与一个E原子的是D.

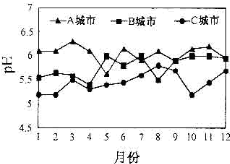 A、B、C三个城市全年雨水的月平均pH变化如图所示.
A、B、C三个城市全年雨水的月平均pH变化如图所示.