题目内容
3.用线桥法标出下列反应中电子转移的方向和数目:(1)Fe+2HCl═FeCl2+H2↑
(2)Fe2O3+3CO$\frac{\underline{\;△\;}}{\;}$2Fe+3CO2.
分析 (1)Fe+2HCl═FeCl2+H2↑反应中,铁元素由0价升高到+2价,氢元素由+1价降到0价,1mol铁参加反应失去2mol电子;
(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2中,Fe元素的化合价由+3价降低为0,C元素的化合价由+2价升高为+4价,1mol氧化铁参加反应失去6mol电子.
解答 解:(1)Fe+2HCl═FeCl2+H2↑反应中,铁元素由0价升高到+2价,氢元素由+1价降到0价,1mol铁参加反应失去2mol电子,则电子转移的方向和数目为: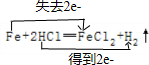 ;
;
故答案为: ;
;
(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2中,Fe元素的化合价由+3价降低为0,C元素的化合价由+2价升高为+4价,1mol氧化铁参加反应失去6mol电子,则电子转移的方向和数目为: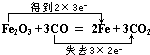 ;
;
故答案为: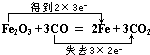 .
.
点评 本题考查氧化还原反应表示方法,准确判断反应中元素的化合价变化为解答的关键,注意双线桥表示方法与单线桥表示区别,题目难度不大.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
13.下列说法正确的是( )
| A. | SiO2是酸性氧化物,它不溶于水也不溶于任何酸 | |
| B. | CO2通入水玻璃中可得硅酸 | |
| C. | 因高温时,SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强 | |
| D. | 石英是制造玻璃的主要原料之一,它在常温下不与NaOH溶液反应 |
11.下列结构图中,●代表前二周期元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键.示例:

根据各图表示的结构特点,下列有关叙述正确的是( )


根据各图表示的结构特点,下列有关叙述正确的是( )
| A. | 通常状况下在水中溶解度丙大于丁 | |
| B. | 甲、乙、丙为非极性分子,丁为极性分子 | |
| C. | 甲的水溶液中存在4种氢键 | |
| D. | 甲中电负性小的元素与丙中电负性大的元素形成的化合物一定不存在极性键 |
12.对反应:2X(g)+Y(g)?2Z(g),减小压强时,对反应产生的影响是( )
| A. | 逆反应速率增大,正反应速率减小 | B. | 逆反应速率减小,正反应速率增大 | ||
| C. | 正、逆反应速率都减小 | D. | 正、逆反应速率都增大 |
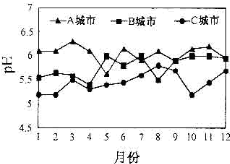 A、B、C三个城市全年雨水的月平均pH变化如图所示.
A、B、C三个城市全年雨水的月平均pH变化如图所示.