题目内容
18.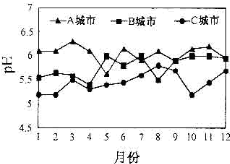 A、B、C三个城市全年雨水的月平均pH变化如图所示.
A、B、C三个城市全年雨水的月平均pH变化如图所示.①受酸雨危害最严重的是C城市.在煤中加入适量石灰石可以大大减少煤燃烧时SO2的排放
②汽车尾气中含有NO2、NO、CO等有害气体.写出由NO2形成硝酸型酸雨的化学方程式3NO2+H2O=2HNO3+NO:
汽车安装尾气净化装置可将NO、CO转化为无害气体,写出该反应的化学方程式2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO3:
分析 ①雨水的pH越小,酸性越强,受酸雨危害越严重;煤中加入适量石灰石,煤燃烧产生的二氧化硫会与碳酸钙分解生成的氧化钙反应生成亚硫酸钙,亚硫酸钙不稳定,被氧气氧化为硫酸钙,即为碳酸钙与氧气、二氧化硫反应生成硫酸钙与二氧化碳.
②二氧化氮与水反应生成硝酸和NO;汽车生产的有害气体为NO、CO,通过催化剂转化为无害气体,反应应生成氮气与二氧化碳,据此写出反应的化学方程式.
解答 解:①由图可知C城市雨水pH最小,故受酸雨危害最严重的是C城市;
煤中加入适量石灰石,煤燃烧产生的二氧化硫与碳酸钙、氧气、二氧化硫反应生成硫酸钙与二氧化碳,反应方程式为:2CaCO3+O2+2SO2$\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+2CO2,从而可以大大减少煤燃烧时SO2的排放,
故答案为:C;石灰石;
②二氧化氮与水反应生成硝酸与NO,反应离子方程式为:3NO2+H2O=2HNO3+NO;
汽车生产的有害气体为NO、CO,通过催化剂转化为无害气体,反应应生成氮气与二氧化碳,反应方程式为:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2,
故答案为:3NO2+H2O=2HNO3+NO;2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
点评 本题考查环境污染与防治、二氧化硫性质等知识,题目难度不大,明确氮的氧化物、硫的氧化物的性质及应用,明确酸雨的成因及治理方法为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
6.现有四种短周期元素:W、X、Y、Z;W、Z的M层均有两个末成对电子,其中W最高化合价和最低化合价代数和为4,X与W位于同一周期,且最外层电子有5种不同的运动状态,Y元素原子的电子占有5个轨道,其中只有一个轨道是单电子,则下列有关比较中正确的是( )
| A. | 第一电离能:Y>X>Z>W | B. | 原子半径:W>X>Z>Y | ||
| C. | 电负性:Y>W>X>Z | D. | 最高正化合价:Y>W>X>Z |
7.下列常用干燥剂,不能干燥氯气的是( )
| A. | 浓硫酸 | B. | 五氧二磷 | C. | 碱石灰 | D. | 氯化钙 |
16.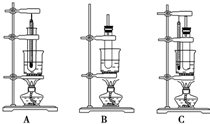 现有三种实验装置,如图,要制备硝基苯,应选用( )
现有三种实验装置,如图,要制备硝基苯,应选用( )
 现有三种实验装置,如图,要制备硝基苯,应选用( )
现有三种实验装置,如图,要制备硝基苯,应选用( )| A. | 装置A | B. | 装置B | C. | 装置C | D. | 都不行 |
 有A、B、C、D、E、F六种短周期元素,其中A 的一种原子不含中子;B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子;C元素的一种气体单质呈蓝色,D与B同周期,该周期中D的简单离子半径最小;E的单质是一种本身有毒可以用来消毒的气体;F 元素最高正价与最低负价的代数和为4.
有A、B、C、D、E、F六种短周期元素,其中A 的一种原子不含中子;B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子;C元素的一种气体单质呈蓝色,D与B同周期,该周期中D的简单离子半径最小;E的单质是一种本身有毒可以用来消毒的气体;F 元素最高正价与最低负价的代数和为4.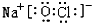 .
.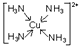 .已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是:共用电子对偏向F而偏离N原子,使得N原子上的孤对电子难于与Cu2+形成配位键.
.已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是:共用电子对偏向F而偏离N原子,使得N原子上的孤对电子难于与Cu2+形成配位键.