20.下列实验操作中正确的是( )
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏时,温度计水银球靠近蒸馏烧瓶的支管口处,且冷却水从冷凝管的上口通入下口流出 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 向1 mol•L-1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体 |
16.甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇.已知某些化学键的键能数据如下表:
请回答下列问题:
(1)已知CO中的C与O之间为叁键连接,则工业制备甲醇的热化学方程式为CO(g)+2H2(g)?CH3OH (g)△H=-116 kJ•mol-1;
(2)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1molCO和 2molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,并用压力计监测容器内压强的变化如下:
则从反应开始到20min时,以CO表示的平均反应速率=0.0125mol/(L•min),该温度下平衡常数K=4(mol/L)-2,若升高温度则K值减小(填“增大”、“减小”或“不变”);
(3)下列描述中能说明上述反应已达平衡的是BC;
A.2v(H2)正=v(CH3OH)逆 B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变 D.单位时间内生成 n molCO 的同时生成 2n molH2.
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
(1)已知CO中的C与O之间为叁键连接,则工业制备甲醇的热化学方程式为CO(g)+2H2(g)?CH3OH (g)△H=-116 kJ•mol-1;
(2)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1molCO和 2molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(3)下列描述中能说明上述反应已达平衡的是BC;
A.2v(H2)正=v(CH3OH)逆 B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变 D.单位时间内生成 n molCO 的同时生成 2n molH2.
14.常温下在水中加入下列物质,不会破坏水的电离平衡的是( )
| A. | 通入HCl气体 | B. | 加入碳酸钠固体 | C. | 加入蔗糖 | D. | 加入金属钠 |
13.工业上用CO生产甲醇的反应为CO(g)+2H2(g)?CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图.下列叙述错误的是( )

0 170102 170110 170116 170120 170126 170128 170132 170138 170140 170146 170152 170156 170158 170162 170168 170170 170176 170180 170182 170186 170188 170192 170194 170196 170197 170198 170200 170201 170202 170204 170206 170210 170212 170216 170218 170222 170228 170230 170236 170240 170242 170246 170252 170258 170260 170266 170270 170272 170278 170282 170288 170296 203614

| A. | CO和H2合成CH3OH的反应:△H<0,△S<0 | |
| B. | 保持温度不变,再充入1molCO和2molH2,反应达到新平衡时$\frac{n(CHOH)}{n(CO)}$减小 | |
| C. | 图1中曲线b可表示使用了催化剂的能量变化情况 | |
| D. | 图3中曲线可表示在不同压强P1、P2(P1<P2)条件下甲醇百分含量随温度变化的情况 |

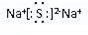 ,所含化学键类型离子键;
,所含化学键类型离子键; 回答下列问题:
回答下列问题: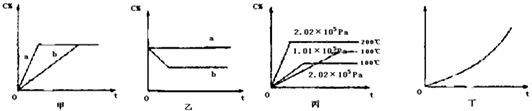

 实验室欲配制980mL0.100mol•L-1Na2CO3溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平
实验室欲配制980mL0.100mol•L-1Na2CO3溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平