题目内容
下列反应的离子方程式书写正确的是( )
| A、用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ |
| B、氯气通入澄清石灰水中:Cl2+2OH-═Cl-+ClO-+H2O |
| C、SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| D、等体积、等物质的量浓度AlCl3与NaOH溶液混合:Al3++4OH-=AlO2-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.发生氧化还原反应生成硝酸铁、S、NO和水;
B.反应生成氯化钙、次氯酸钙和水;
C.发生氧化还原反应生成硫酸钠和盐酸;
D.等体积、等物质的量浓度,碱不足,生成氢氧化铝.
B.反应生成氯化钙、次氯酸钙和水;
C.发生氧化还原反应生成硫酸钠和盐酸;
D.等体积、等物质的量浓度,碱不足,生成氢氧化铝.
解答:
解:A.用稀HNO3溶解FeS固体的离子反应为FeS+NO3-+4H+═Fe3++S+NO↑+2H2O,故A错误;
B.氯气通入澄清石灰水中的离子反应为Cl2+2OH-═Cl-+ClO-+H2O,故B正确;
C.SO2气体通入NaClO溶液中的离子反应为SO2+ClO-+H2O═SO42-+2H++Cl-,故C错误;
D.等体积、等物质的量浓度AlCl3与NaOH溶液混合的离子反应为Al3++3OH-=Al(OH)3↓,故D错误;
故选B.
B.氯气通入澄清石灰水中的离子反应为Cl2+2OH-═Cl-+ClO-+H2O,故B正确;
C.SO2气体通入NaClO溶液中的离子反应为SO2+ClO-+H2O═SO42-+2H++Cl-,故C错误;
D.等体积、等物质的量浓度AlCl3与NaOH溶液混合的离子反应为Al3++3OH-=Al(OH)3↓,故D错误;
故选B.
点评:本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及复分解反应的离子反应考查,题目难度中等.

练习册系列答案
相关题目
下列物质在水溶液中既能电离又能水解的是( )
| A、NH4Cl |
| B、NaHS |
| C、HNO3 |
| D、HClO |
下列实验设计或实验操作中,正确的是( )
A、 铜与浓硝酸反应制取NO2 |
B、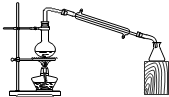 该装置设计合理,可实现石油的分馏 |
C、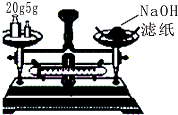 称量25g氢氧化钠 |
D、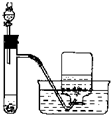 H2O2溶液与MnO2制备O2 |
下列离子方程式中正确的是( )
| A、稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| B、用小苏打治疗胃酸过多:HCO3-+H+═H2O+CO2↑ |
| C、硝酸滴在石灰石上:CaCO3+2H+═Ca2++H2CO3 |
| D、醋酸钠和盐酸混和:CH3COONa+H+═CH3COOH+Na+ |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol Cl2与足量的铁反应,转移的电子数为3NA |
| B、在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
| C、将pH=2的盐酸和pH=4的硫酸等体积混合,所得溶液pH=3 |
| D、1mol OH-和1mol-OH(羟基)中含有的质子数均为9NA |
下列微粒中能影响水的电离平衡,且使水的电离平衡向左移动的是( )
| A、SO42- |
| B、Cl- |
| C、Na+ |
D、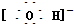 |
R为短周期元素,其原子所具有的电子层数为最外层电子数的一半.下列说法中不正确的是( )
A、当它形成含氧酸根离子R2O
| ||||
B、当它形成含氧酸根离子RO
| ||||
C、当它形成含氧酸根离子RO
| ||||
D、当它形成含氧酸根离子R2O
|
下列有关说法正确的是( )
| A、使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 |
| B、化学反应有新物质生成,并遵循质量守恒定律和能量守恒定律 |
| C、HCl和NaOH反应的中和热△H=-57.3kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=-114.6kJ?mol-1 |
| D、500℃、300MPa下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ?mol-1 |