题目内容
下列微粒中能影响水的电离平衡,且使水的电离平衡向左移动的是( )
| A、SO42- |
| B、Cl- |
| C、Na+ |
D、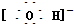 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:水的电离H2O?H++OH-,加入酸或碱抑制水的电离,加入能水解的盐促进水的电离,
A.硫酸氢根离子在水溶液中完全电离,电离出氢离子和硫酸根离子,抑制了水的电离,水的电离向逆反应方向移动;
B.盐酸为强电解质,氯离子为盐酸的阴离子,不水解,对水的电离无影响;
C.该微粒核外18个电子,是原子失去1个电子形成的,是钾离子,钾离子不水解,对水的电离无影响;
D.该微粒为硫离子,硫离子是弱酸氢硫酸的阴离子,在水中水解,生成氢硫酸,能使水的电离平衡向右移动,促进了水的电离.
A.硫酸氢根离子在水溶液中完全电离,电离出氢离子和硫酸根离子,抑制了水的电离,水的电离向逆反应方向移动;
B.盐酸为强电解质,氯离子为盐酸的阴离子,不水解,对水的电离无影响;
C.该微粒核外18个电子,是原子失去1个电子形成的,是钾离子,钾离子不水解,对水的电离无影响;
D.该微粒为硫离子,硫离子是弱酸氢硫酸的阴离子,在水中水解,生成氢硫酸,能使水的电离平衡向右移动,促进了水的电离.
解答:
解:水的电离H2O?H++OH-,加入酸或碱抑制水的电离,加入能水解的盐促进水的电离,
A.硫酸根离子在水溶液中对水的电离无影响,水的电离平衡H2O?H++OH-不移动,故A错误;
B.氯离子为强酸盐酸的阴离子,Cl-不水解,不会影响水的电离,故B错误;
C.Na+离子是强碱氢氧化钠的阳离子,不水解,对水的电离无影响,故C错误;
D.氢氧根离子是显碱性的离子,抑制水的电离,且能使水的电离平衡向左移动,故D正确;
故选D.
A.硫酸根离子在水溶液中对水的电离无影响,水的电离平衡H2O?H++OH-不移动,故A错误;
B.氯离子为强酸盐酸的阴离子,Cl-不水解,不会影响水的电离,故B错误;
C.Na+离子是强碱氢氧化钠的阳离子,不水解,对水的电离无影响,故C错误;
D.氢氧根离子是显碱性的离子,抑制水的电离,且能使水的电离平衡向左移动,故D正确;
故选D.
点评:本题主要考查了水的电离,题目难度不大,注意解答须抓住酸或碱抑制水的电离,加入能水解的盐促进水的电离,试题有利于调动学生的学习兴趣和学习积极性,提高学生灵活应用所学知识解决实际问题的能力.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
反应N2+3H2═2NH3+Q(Q>0),决定该反应速率的最主要因素是( )
| A、N2、H2的性质 |
| B、温度 |
| C、压强 |
| D、催化剂 |
下列反应中,属于取代反应的是( )
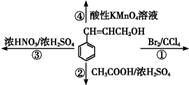

| A、①② | B、②③ | C、③④ | D、①④ |
在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A、若增加CO的用量,上式中的△H增大 |
| B、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| C、若升高温度,则正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| D、达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |
下列反应的离子方程式书写正确的是( )
| A、用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ |
| B、氯气通入澄清石灰水中:Cl2+2OH-═Cl-+ClO-+H2O |
| C、SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| D、等体积、等物质的量浓度AlCl3与NaOH溶液混合:Al3++4OH-=AlO2-+H2O |
下列说法不正确的是( )
| A、常温下,向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) |
| B、将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 |
| C、pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 |
| D、0.2mol?L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
有关能源的说法不正确的是( )
| A、煤、石油、天然气均为化石燃料 |
| B、化石能源是非再生能源 |
| C、氢能是可再生能源 |
| D、氢能、核能均是无污染的高效能源 |