题目内容
下列实验设计或实验操作中,正确的是( )
A、 铜与浓硝酸反应制取NO2 |
B、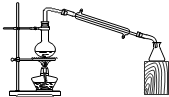 该装置设计合理,可实现石油的分馏 |
C、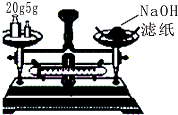 称量25g氢氧化钠 |
D、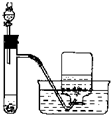 H2O2溶液与MnO2制备O2 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.二氧化氮与水反应;
B.石油的分馏,需要温度计;
C.NaOH易潮解,具有腐蚀性;
D.H2O2溶液与MnO2混合反应生成水和氧气,为固液反应不需要加热的反应原理.
B.石油的分馏,需要温度计;
C.NaOH易潮解,具有腐蚀性;
D.H2O2溶液与MnO2混合反应生成水和氧气,为固液反应不需要加热的反应原理.
解答:
解:.二氧化氮与水反应,则不能利用排水法收集二氧化氮,故A错误;
B.石油的分馏,需要温度计,则应利用蒸馏烧瓶及温度计,温度计在烧瓶的支管口处,故B错误;
C.NaOH易潮解,具有腐蚀性,则NaOH应在小烧杯中称量,且物体在左盘,砝码在右盘,故C错误;
D.H2O2溶液与MnO2混合反应生成水和氧气,为固液反应不需要加热的反应原理,图中制备装置合理,故D正确;
故选D.
B.石油的分馏,需要温度计,则应利用蒸馏烧瓶及温度计,温度计在烧瓶的支管口处,故B错误;
C.NaOH易潮解,具有腐蚀性,则NaOH应在小烧杯中称量,且物体在左盘,砝码在右盘,故C错误;
D.H2O2溶液与MnO2混合反应生成水和氧气,为固液反应不需要加热的反应原理,图中制备装置合理,故D正确;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、固体称量及常见气体的制备实验为解答的关键,侧重学生分析能力及知识综合应用能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在密闭容器中,对于反应2NO2(g)?N2O4(g)△H<0,增大压强(体积迅速减小),下列说法正确的是 ( )
| A、平衡逆向移动 |
| B、混合气体颜色比原来深 |
| C、混合气体颜色比原来浅 |
| D、混合气体的平均相对分子质量变小 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、由水电离产生的c(H+)=10-12mol/L的溶液:Na+、K+、NO3-、SO42- |
| B、明矾溶液:K+、C1-、S2-、OH- |
| C、pH=1的溶液:Ag(NH3)2+、Fe3+、ClO4-、NO3- |
| D、能溶解Al2O3的溶液:Na+、Mg2+、HCO3-、SO42- |
 3-甲基香豆素有香草味,可用于香料及化妆品,其结构简式如图所示.关于它的说法正确的是( )
3-甲基香豆素有香草味,可用于香料及化妆品,其结构简式如图所示.关于它的说法正确的是( )| A、分子式为C10H10O2 |
| B、分子中所有原子可能在同一平面上 |
| C、1mol该有机物与Br2的CCl4溶液发生加成反应,可以消耗5mol Br2 |
| D、1mol该有机物与NaOH溶液反应,可以消耗2mol NaOH |
下列有关氧化还原反应的叙述中正确的是( )
| A、有单质参加或有单质生成的反应一定是氧化还原反应 |
| B、金属单质在化学反应中一定作还原剂 |
| C、失电子的反应物在反应中作氧化剂,反应中被还原 |
| D、氧化还原的本质是元素化合价的升降 |
下列反应中,属于取代反应的是( )
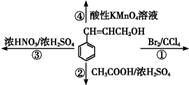

| A、①② | B、②③ | C、③④ | D、①④ |
常温下,在密闭容器中分别充入两种气体各0.1mol,在一定条件下充分反应后,恢复到原温度时,压强和开始时相同.则原混合气体可能为( )
| A、H2和O2 |
| B、HCl和NH3 |
| C、H2和Cl2 |
| D、CO和O2 |
下列反应的离子方程式书写正确的是( )
| A、用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ |
| B、氯气通入澄清石灰水中:Cl2+2OH-═Cl-+ClO-+H2O |
| C、SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| D、等体积、等物质的量浓度AlCl3与NaOH溶液混合:Al3++4OH-=AlO2-+H2O |