题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol Cl2与足量的铁反应,转移的电子数为3NA |
| B、在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
| C、将pH=2的盐酸和pH=4的硫酸等体积混合,所得溶液pH=3 |
| D、1mol OH-和1mol-OH(羟基)中含有的质子数均为9NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、氯气和足量铁反应生成氯化铁,电子转移依据氯气计算;
B、铝离子水溶液中水解;
C、依据酸酸混合后溶液PH计算方法计算分析;
D、依据氢氧根离子和甲基结构计算质子数;
B、铝离子水溶液中水解;
C、依据酸酸混合后溶液PH计算方法计算分析;
D、依据氢氧根离子和甲基结构计算质子数;
解答:
解:A、氯气和足量铁反应生成氯化铁,电子转移依据氯气反应的物质的量计算,转移的电子数为2NA,故A错误;
B、铝离子水溶液中水解,在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA ,故B错误;
C、将pH=2的盐酸和pH=4的硫酸等体积混合,氢离子浓度=
,所得溶液pH=-lgc(H+)≈2.3,故C错误;
D、1mol OH-和1mol-OH(羟基)中,所含电子数不同,质子数相同,含有的质子数均为9NA,故D正确;
故选D.
B、铝离子水溶液中水解,在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA ,故B错误;
C、将pH=2的盐酸和pH=4的硫酸等体积混合,氢离子浓度=
| 10-2+10-4 |
| 2 |
D、1mol OH-和1mol-OH(羟基)中,所含电子数不同,质子数相同,含有的质子数均为9NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是氧化还原反的应电子转移计算,溶液PH计算方法,微粒结构的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列实验操作能够达到目的是( )
| A、用托盘天平称取25.20g NaCl固体 |
| B、用湿润的蓝色石蕊试纸检验NH3 |
| C、用湿润的pH试纸测定某溶液的pH |
| D、用25mL碱式滴定管量取14.80mL 1mol/L NaOH溶液 |
下列有关氧化还原反应的叙述中正确的是( )
| A、有单质参加或有单质生成的反应一定是氧化还原反应 |
| B、金属单质在化学反应中一定作还原剂 |
| C、失电子的反应物在反应中作氧化剂,反应中被还原 |
| D、氧化还原的本质是元素化合价的升降 |
常温下,在密闭容器中分别充入两种气体各0.1mol,在一定条件下充分反应后,恢复到原温度时,压强和开始时相同.则原混合气体可能为( )
| A、H2和O2 |
| B、HCl和NH3 |
| C、H2和Cl2 |
| D、CO和O2 |
下列说法正确的是( )
| A、实验室从海带提取单质碘的方法依次是:取样、灼烧、溶解、过滤、萃取 |
| B、氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中 |
| C、用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 |
| D、油脂在碱性条件下的水解反应称为油脂的氢化,又称为油脂的硬化 |
下列反应的离子方程式书写正确的是( )
| A、用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ |
| B、氯气通入澄清石灰水中:Cl2+2OH-═Cl-+ClO-+H2O |
| C、SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| D、等体积、等物质的量浓度AlCl3与NaOH溶液混合:Al3++4OH-=AlO2-+H2O |
固体NH5属于离子晶体.它与水反应的化学方程式为NH5+H2O→NH3?H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气.下列有关NH5叙述正确的是( )
| A、含有NH4+和H- |
| B、NH5中N元素的化合价为+5价 |
| C、1mol NH5中含有5NA个N-H键 |
| D、与乙醇反应时,NH5被还原 |
用如图所示装置进行实验,装置正确且设计合理的是( )

| A、用图①所示装置收集HCl气体 |
| B、用图②所示装置配制一定物质的量浓度的硫酸 |
| C、用图③所示装置检查该装置的气密性 |
| D、用图④所示装置进行实验室制取的实验 |
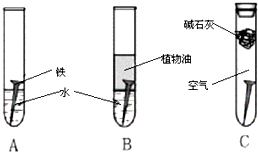 某研究小组对铁生锈进行研究:
某研究小组对铁生锈进行研究: