题目内容
下列离子方程式中正确的是( )
| A、稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| B、用小苏打治疗胃酸过多:HCO3-+H+═H2O+CO2↑ |
| C、硝酸滴在石灰石上:CaCO3+2H+═Ca2++H2CO3 |
| D、醋酸钠和盐酸混和:CH3COONa+H+═CH3COOH+Na+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.Cu与稀硫酸不反应;
B.反应生成氯化钠、水和二氧化碳;
C.反应生成硝酸钙、水和二氧化碳;
D.醋酸钠为强电解质.
B.反应生成氯化钠、水和二氧化碳;
C.反应生成硝酸钙、水和二氧化碳;
D.醋酸钠为强电解质.
解答:
解:A.不反应,则不能书写离子反应,故A错误;
B.用小苏打治疗胃酸过多的离子反应为HCO3-+H+═H2O+CO2↑,故B正确;
C.硝酸滴在石灰石上的离子反应为CaCO3+2H+═Ca2++H2O+CO2↑,故C错误;
D.醋酸钠和盐酸混和的离子反应为CH3COO-+H+═CH3COOH,故D错误;
故选B.
B.用小苏打治疗胃酸过多的离子反应为HCO3-+H+═H2O+CO2↑,故B正确;
C.硝酸滴在石灰石上的离子反应为CaCO3+2H+═Ca2++H2O+CO2↑,故C错误;
D.醋酸钠和盐酸混和的离子反应为CH3COO-+H+═CH3COOH,故D错误;
故选B.
点评:本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
常温下,对pH=10的NaHCO3溶液中,各微粒的物质的量浓度分析正确的是( )
| A、c(CO32-)>c(H2CO3) |
| B、c(Na+)>c(HCO3-)>c(H+)>c(OH-) |
| C、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| D、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
 3-甲基香豆素有香草味,可用于香料及化妆品,其结构简式如图所示.关于它的说法正确的是( )
3-甲基香豆素有香草味,可用于香料及化妆品,其结构简式如图所示.关于它的说法正确的是( )| A、分子式为C10H10O2 |
| B、分子中所有原子可能在同一平面上 |
| C、1mol该有机物与Br2的CCl4溶液发生加成反应,可以消耗5mol Br2 |
| D、1mol该有机物与NaOH溶液反应,可以消耗2mol NaOH |
下列反应中,属于取代反应的是( )
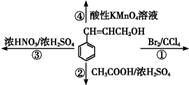

| A、①② | B、②③ | C、③④ | D、①④ |
常温下,在密闭容器中分别充入两种气体各0.1mol,在一定条件下充分反应后,恢复到原温度时,压强和开始时相同.则原混合气体可能为( )
| A、H2和O2 |
| B、HCl和NH3 |
| C、H2和Cl2 |
| D、CO和O2 |
在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A、若增加CO的用量,上式中的△H增大 |
| B、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| C、若升高温度,则正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| D、达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |
下列反应的离子方程式书写正确的是( )
| A、用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ |
| B、氯气通入澄清石灰水中:Cl2+2OH-═Cl-+ClO-+H2O |
| C、SO2气体通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| D、等体积、等物质的量浓度AlCl3与NaOH溶液混合:Al3++4OH-=AlO2-+H2O |
有关能源的说法不正确的是( )
| A、煤、石油、天然气均为化石燃料 |
| B、化石能源是非再生能源 |
| C、氢能是可再生能源 |
| D、氢能、核能均是无污染的高效能源 |