题目内容
3.铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途.下列关于铝的说法不正确的是( )| A. | 铝的表面容易形成致密的氧化膜,抗腐蚀性能好 | |
| B. | 常温下不与任何碱反应 | |
| C. | 铝元素在地壳中的含量高,储量丰富 | |
| D. | 工业上可以用电解法冶炼铝 |
分析 A.金属铝易被氧气氧化形成致密的氧化铝保护膜;
B.铝能够与强碱的溶液发生反应;
C.铝在地壳中含量占第3位;
D.工业上用电解熔融的氧化铝冶炼铝.
解答 解:A.金属铝易被氧气氧化形成致密的氧化膜氧化铝,抗腐蚀性能好,故A正确;
B.常温下,铝能够与氢氧化钠溶液反应生成偏铝酸钠和氢气,故B错误;
C.铝在地壳中含量占第3位,储量丰富,故C正确;
D.工业上用电解熔融的氧化铝冶炼铝,故D正确;
故选:B.
点评 本题考查了铝的性质,熟悉铝的化学性质及其在地壳中的含量是解题关键,注意金属冶炼的方法的选择.

练习册系列答案
相关题目
19.有钠、镁、铝各n mol,分别与等体积、均与含xmolHCl的盐酸反应,下列说法不正确的是( )
| A. | x<n时,钠生成的氢气最多 | B. | x=n时,钠、镁、铝生成的氢气一样多 | ||
| C. | n<x≤2n时,生成的氢气钠<镁=铝 | D. | x≥2n时,生成的氢气钠<镁<铝 |
14.X、Y是元素周期表中同一周期的两种元素,下列叙述能说明X的原子失电子能力比Y强的是( )
| A. | X原子的最外层电子数比Y原子的最外层电子数多 | |
| B. | 原子半径:X>Y | |
| C. | 1mol X从酸中置换出来的氢比1mol Y从酸中置换出来的氢多 | |
| D. | X原子的最高正化合价比Y原子的最高正化合价高 |
15.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与2.24LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A. | 40mL | B. | 60mL | C. | 80mL | D. | 100mL |
13.实验室中,下列除去括号内杂质的有关操作正确的是( )
| A. | 苯(硝基苯):加少量蒸馏水振荡,待分层后分液 | |
| B. | CO2(HCl、水蒸气):通过盛有碱石灰的干燥管 | |
| C. | 乙烷(乙烯):通入氢气发生加成反应 | |
| D. | 乙醇(水):加新制的生石灰,蒸馏 |
 某校化学兴趣小组利用在加热条件下浓盐酸与二氧化锰的反应来制取并收集氯气,实验装置如图所示.
某校化学兴趣小组利用在加热条件下浓盐酸与二氧化锰的反应来制取并收集氯气,实验装置如图所示.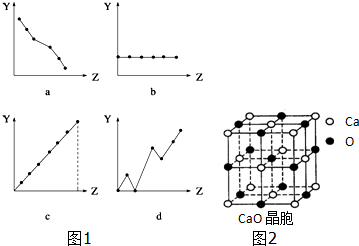
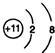 ;
; ;仅由极性键形成的非极性分子的结构式为
;仅由极性键形成的非极性分子的结构式为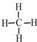 ,该分子中心原子的杂化轨道类型是sp3杂化;简单氢化物的沸点最高的是H2O.
,该分子中心原子的杂化轨道类型是sp3杂化;简单氢化物的沸点最高的是H2O.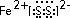 .
.