题目内容
5.下列有机化合物分子中的所有碳原子不可能处于同一平面的是.| A. | 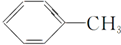 | B. | HC≡C-CH3 | ||
| C. | 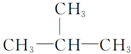 | D. | 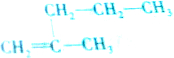 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断.
解答 解:A、苯为平面结构,甲苯中甲基碳原子处于苯中H原子位置,所有碳原子都处在同一平面上,故A不符合;
B、乙炔为直线结构,丙炔中甲基碳原子处于乙炔中H原子位置,所有碳原子处于同一直线,所有碳原子都处在同一平面上,故B不符合;
C、2-甲基丙烷中,3个甲基处于2号碳原子四面体的顶点位置,2号碳原子处于该四面体内部,所以碳原子不可能处于同一平面,故C符合;
D、2-甲基-1-戊烯中,双键两端的碳原子所连的碳原子都在同一个平面上,乙基上的碳原子可以和它们共面,故D不符合;
故选C.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.

练习册系列答案
相关题目
11.同一温度下,A物质10g溶于50g水中成饱和溶液,B物质的饱和溶液的质量分数为30%,C物质的溶质分别蒸发10g水,第一次析出2g晶体,第二次析出4g晶体,则A、B、C三种物质的溶解度大小顺序为( )
| A. | A>B>C | B. | A<B<C | C. | C>A>B | D. | B>C>A |
16.对于相应化学用语的推论合理的是( )
| 选项 | 化学用语 | 推论 |
| A | ${\;}_{92}^{238}{U}^{3+}$ | 该轴离子核外有89个电子 |
| B | 2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ•mol | 1mol氢气完全燃烧放出热量483.6kJ |
| C | 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2+Cl2↑ | NaCl氧化性Cl2强 |
| D | FeO+4H++HNO3-=Fe3++NO2↑+2H2O | 氧化亚铁溶于稀硝酸的离子方程式 |
| A. | A | B. | B | C. | C | D. | D |
13.某学生在实验室进行化学实验,其中他的操作不正确的是( )
| A. | 取用AgNO3时,应在实验柜中寻找棕色瓶带有滴管的试剂瓶 | |
| B. | 用稀HNO3清洗做过银镜反应后的试管 | |
| C. | 用NaOH溶液清洗沾有硫磺的试管 | |
| D. | 用稀HCl清洗做过高锰酸钾分解实验的试管 |
20.反应2SO2(g)+O2(g)?2SO3(g)经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L•s),则这段时间为( )
| A. | 0.1 s | B. | 2.5 s | C. | 10 s | D. | 5 s |
10.常温下,将NO和O2两种气体按物质的量1:3混合,则其平均相对分子质量是( )
| A. | 40.7 | B. | 46 | C. | 36 | D. | 44 |
17.下列说法正确的是( )
| A. | 3≤原子最外层电子数<8的元素一定是非金属元素 | |
| B. | 原子最外层只有1个电子的元素一定是第ⅠA族元素 | |
| C. | 最外层电子数比次外层电子数多的元素一定是第2周期元素 | |
| D. | 某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第3周期 |

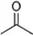 ,根据键线式回答下列问题:
,根据键线式回答下列问题: 分子式:C5H9O2,结构简式:CH2=CH(CH3)COOCH3.
分子式:C5H9O2,结构简式:CH2=CH(CH3)COOCH3. .
.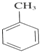 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$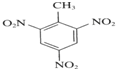 +3H2O.
+3H2O. 的一氯取代物有2种,
的一氯取代物有2种,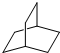 的二氯取代物有7种.
的二氯取代物有7种.