题目内容
11.同一温度下,A物质10g溶于50g水中成饱和溶液,B物质的饱和溶液的质量分数为30%,C物质的溶质分别蒸发10g水,第一次析出2g晶体,第二次析出4g晶体,则A、B、C三种物质的溶解度大小顺序为( )| A. | A>B>C | B. | A<B<C | C. | C>A>B | D. | B>C>A |
分析 同一温度下溶质溶解度相同,饱和溶液中:溶质质量:溶剂质量=溶解度:100,溶质质量分数=$\frac{S}{100+S}$×100%,C物质的溶质分别蒸发10g水,第一次析出2g晶体,第二次析出4g晶体,说明蒸发10g水析出4g晶体,依据饱和溶液组成计算溶解度.
解答 解:饱和溶液中:溶质质量:溶剂质量=溶解度:100,A物质10g溶于50g水中成饱和溶液,溶解度S1:100=10:50,S1=20g,
B物质的饱和溶液的质量分数为30%,溶质质量分数=$\frac{{S}_{2}}{100+{S}_{2}}$×100%=30%,S2=42.9g,
C物质的溶质分别蒸发10g水,第一次析出2g晶体,第二次析出4g晶体,说明蒸发10g水析出4g晶体,依据饱和溶液组成计算溶解度,4:10=S3:100,S3=40g;
S2>S3>S1,即则A、B、C三种物质的溶解度大小顺序为B>C>A.
故选D.
点评 本题考查了溶质溶解度概念的理解应用和计算分析,注意饱和溶液组成的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
1.下列有关化学用语使用正确的是( )
| A. | NH4Br的电子式: | |
| B. | CO2的比例模型: | |
| C. | CCl4分子构型为正四面体,其键与键之间的夹角为109°28′ | |
| D. | 中子数为20的氯原子:20Cl |
6.由丙烷、乙烯、乙炔组成的混合气体,完全燃烧后生成CO2和H2O的物质的量相同,原混合气体中三种烃的体积之比不可能是( )
| A. | 1:2:1 | B. | 3:2:3 | C. | 2:5:2 | D. | 1:2:3 |
4.四种常见元素的性质或结构信息如F表所示,请问答下列问题.
(1)R的基态原子价层电子排布式为3d104s1,这四种元素的第一电离能由大到小的顺序为N>C>Si>Cu(写元素符号).
(2)A、B,D均可形成多种氢化物,在最常见的三种氢化物中,分子构型为三角锥的氢化物分子式为NH3,任意写出一种中心原子存在sp2、sp3两种杂化类型的物质的结构简式CH2=CH-CH3,与A的常见单质互为等电子体的上述元素的氧化物是CO.
(3)B、D均可形成氧化物,等物质的量的B、D的最高价氧化物中σ键之比为2:1,已知有下列两种数据:
请解释键能大小与两种氧化物熔点、沸点高低差异过大的原因CO2是分子晶体,熔点、沸点高低是由比较微弱的范德华力决定的,而与化学键强弱无关,SiO2属原子晶体,其熔点、沸点高低是由强大的共价键决定的
(4)在一定条件下,Cl-与R2+可形成一种无限长链离子 ,研究表明•
,研究表明•
该离子中每个氯原子最外层均达到8电子稳定结构,有些氧与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为${(CuC{l}_{3})}_{n}^{n-}$.
(5)A元素能形成组成为Pt(AH3)2Cl2 的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不 具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大.
①Q是非极性(填“极性”或“非极性”)分子,
②P的结构简式为 ( AH3配体作为一个整体写).
( AH3配体作为一个整体写).
| 元素 | A | B | R | D |
| 相关信息 | 基态原子核外电子占据3个能级且最高能级上有3个电子 | B的单质是最常见半导体材料 | 位于第四周期ⅠB族 | 是非金属元素,其形成的某种单质是电的良导体,有的分子形状似足球 |
(2)A、B,D均可形成多种氢化物,在最常见的三种氢化物中,分子构型为三角锥的氢化物分子式为NH3,任意写出一种中心原子存在sp2、sp3两种杂化类型的物质的结构简式CH2=CH-CH3,与A的常见单质互为等电子体的上述元素的氧化物是CO.
(3)B、D均可形成氧化物,等物质的量的B、D的最高价氧化物中σ键之比为2:1,已知有下列两种数据:
| 键能(kJ/mol) | 熔点(K) | 沸点(K) | |
| BO2 | B-O:452 | 1923 | 2503 |
| DO2 | D=O:615,D-O:348 | 216 | 195 |
(4)在一定条件下,Cl-与R2+可形成一种无限长链离子
 ,研究表明•
,研究表明•该离子中每个氯原子最外层均达到8电子稳定结构,有些氧与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为${(CuC{l}_{3})}_{n}^{n-}$.
(5)A元素能形成组成为Pt(AH3)2Cl2 的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不 具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大.
①Q是非极性(填“极性”或“非极性”)分子,
②P的结构简式为
 ( AH3配体作为一个整体写).
( AH3配体作为一个整体写).
5.下列有机化合物分子中的所有碳原子不可能处于同一平面的是.
| A. | 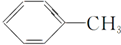 | B. | HC≡C-CH3 | ||
| C. | 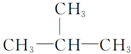 | D. | 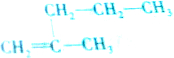 |
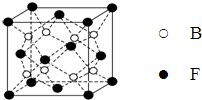 已知A、B、C、D、E、F、G、H、I为元素周期表中原子序数依次增大的前四周期元素,A原子的最外层中p轨道上的电子数等于前一电子层电子总数;A、B、C、D;E、F与G分别位于同一周期.C原子L层上有2对成电子,D、E、F的核外电子排布相同的简单离子可形成一种E3FD6型离子晶体X,EG、HC为电子数相同的离子晶体.I原子M层为全充满状态,且核外的未成对电子只有一个.请根据以上情况,回答下列问题:(答题时,用对应的元素符号表示)
已知A、B、C、D、E、F、G、H、I为元素周期表中原子序数依次增大的前四周期元素,A原子的最外层中p轨道上的电子数等于前一电子层电子总数;A、B、C、D;E、F与G分别位于同一周期.C原子L层上有2对成电子,D、E、F的核外电子排布相同的简单离子可形成一种E3FD6型离子晶体X,EG、HC为电子数相同的离子晶体.I原子M层为全充满状态,且核外的未成对电子只有一个.请根据以上情况,回答下列问题:(答题时,用对应的元素符号表示)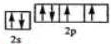 ;H离子电子排布式1s22s22p63s23p6;I位于周期表ds区;D在周期表中的位置第二周期ⅤⅡA族
;H离子电子排布式1s22s22p63s23p6;I位于周期表ds区;D在周期表中的位置第二周期ⅤⅡA族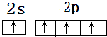 ,不符合能量最低原理原理.
,不符合能量最低原理原理.