题目内容
已知A、B、C、D、E、F、G位于元素周期表的前四周期,且元素原子序数依次增加,A焰色反应呈黄色;工业常用电解B的熔融的氯化物来制备B,C是一种能被HF和NaOH溶液溶解的单质,D的电负性比磷大,第一电离能却比磷小,E单质是制备漂白液的原料,F能形成红色(或砖红色)和黑色的两种氧化物,G是一种主族金属。
(1)前四周期所有元素中,基态原子中未成对电子与其所在周期数相同的元素有 种。
(2)元素A、B、C分别与氟气化合形成物质X、Y、Z熔点见下表:
| 氟化物 | X | Y | Z |
| 熔点/K | 1266 | 1534 | 183 |
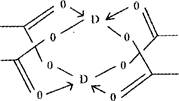
(3)已知常温条件下,极性分子DOE2是一种液态化合物,中心原子D的杂化方式是 。向盛有10mL水的锥形瓶中滴加少量的DOE2溶液,生成两种有刺激性气味的气体。请书写此反应的化学方程式 。
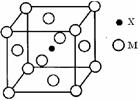
(4)G与氮原子可1:1化合,形成人工合成的新型半导体材料,其晶体结构与单晶硅相似。G原子的价电子排布式为 。在该合成材料中,与同一个G原子相连的N原子构成的空间构型为正四面体。在四种基本晶体类型中,此晶体属于 晶体。
(5)F晶体的堆积方式是 (填堆积名称),其配位数为 。 向F的硫酸盐溶液中滴加氨水直至过量,写出此过程所涉及的两个离子方程式 根据价层电子对互斥理论,预测SO42-的空间构型为 。
(1)5(1分)
(2)NaF和MgF2为离子晶体,SiF4为分子晶体,(1分) MgF2的晶格能大于NaF(1分) (3)SP3(1分) SOCl2 + H2O = SO2↑+ 2HCl↑(2分)
(4)4s2p1(1分),原子(1分)
(5)面心立方最密堆积(1分), 12(1分), Cu2+ + 2NH3·H2O = Cu(OH)2↓+ 2NH4+(2分)Cu(OH)2 + 4NH3·H2O = [Cu(NH3)4]2+ + 4H2O + 2OH-(或将NH3·H2O写成NH3)(2分), 正四面体(1分)
解析试题分析:A、B、C、D、E、F、G位于元素周期表的前四周期,且元素原子序数依次增加,A焰色反应呈黄色是Na;工业常用电解B的熔融的氯化物来制备B,是Mg;C是一种能被HF和NaOH溶液溶解的单质,是Si;D的电负性比磷大,第一电离能却比磷小,是S;E单质是制备漂白液的原料,为Cl;F能形成红色(或砖红色)和黑色的两种氧化物,为Cu;G是一种主族金属。
(1)前四周期所有元素中,基态原子中未成对电子与其所在周期数相同的元素有1s1,2s22p2或2s22p4,3s23p3,3d64s2(注意根据洪特规则3d44s2是3d54s1),共5种。
(2)元素Na、Mg、Si分别与氟气化合形成物质X(NaF)、Y(MgF2)、Z(SiF4)熔点NaF和MgF2为离子晶体,SiF4为分子晶体,MgF2的晶格能大于NaF。
(3)已知常温条件下,极性分子SOCl2是一种液态化合物,中心原子S有价层电子4对,杂化方式是SP3。向盛有10mL水的锥形瓶中滴加少量的SOCl2溶液,生成两种有刺激性气味的气体为水解,即SO2和HCl。
(4)G与氮原子可1:1化合,形成人工合成的新型半导体材料,其晶体结构与单晶硅相似。物质分子式是GN,G为+3价,在Cu之后,故是G原子的价电子排布式为4s2p1。在该合成材料中,与同一个G原子相连的N原子构成的空间构型为正四面体。在四种基本晶体类型中,此晶体属于原子晶体。
(5)Cu晶体的堆积方式是面心立方最密堆积,其配位数为12。 向CuSO4溶液中滴加氨水直至过量,Cu2+先生成Cu(OH)2沉淀,在溶解为[Cu(NH3)4]2+,根据价层电子对互斥理论,SO42-的价层电子为4对,空间构型为正四面体。
考点:物质结构与性质。

 阅读快车系列答案
阅读快车系列答案(12分)有A、B、C、D、E五种原子序数小于18的元素,其特征信息如下:
| 元素编号 | 特征信息 |
| A | 其中一种原子核内只有质子没有中子 |
| B | 其原子的L层电子数是K层的3倍 |
| C | 其阳离子与B的阴离子具有相同的电子层结构, 且核电荷数与B相差3 |
| D | 其原子的最外层电子数等于电子层数,且是地壳 中含量较多的元素之一 |
| E | 单质为黄绿色气体,可用于制造漂白粉 |
(1)由A、B、C三种元素形成的化合物含有的化学键类型是 。
(2)由A、B、C元素中两两组合形成的化合物相互反应生成单质的化学方程
式 。
(3)D单质与由A、B、C三种元素形成的化合物的水溶液反应的离子方程式
。
(4)写出实验室用软锰矿(MnO2)制取E的化学方程式 。
(5)C和D两元素形成的单质活泼些较强的是 (写元素符号),判断依据是 。
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N元素的电负性由大到小的顺序是 ,
C60和金刚石都是碳的同素异形体,二者相比,熔点高的是 ,原因是 。
(2)A、B均为短周期金属元素,依据表中数据,写出B的基态原子的电子排布式: 。
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
[Mn(H2O)6]2+ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为
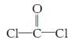 ,每个COCl2分子内含有 个σ键, 个π键,其中心原子采取 杂化轨道方式。
,每个COCl2分子内含有 个σ键, 个π键,其中心原子采取 杂化轨道方式。②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)。反应过程中,断裂的化学键只有配位键,则形成的化学键类型是 。
(13分)下图是元素周期表的一部分,表中的①—⑩中元素,用化学用语填空回答:
| 族 周期 | I A | IIA | IIIA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 二 | | | | ① | ② | | ③ | |
| 三 | | ④ | ⑤ | ⑥ | | | ⑦ | ⑧ |
| 四 | ⑨ | | | | | | ⑩ | |
(1)在这些元素中,⑩原子的原子结构示意图为 。
(2)写出①的最高价氧化物和②的单质的电子式 , 。
(3)用电子式表示③与④形成化合物的过程 。
(4)①的单质和⑥的氧化物反应的化学方程式 。
(5)写出⑤的单质与氢氧化钠反应的化学方程式:
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式: 。
(6)已知拆开l mol C—H键、l mol O=O键、l molC=O键、l mol H—O键分别需要吸收的能量为414kJ、498kJ、728kJ、464kJ。则l mol甲烷完全燃烧放出 kJ的热量。
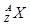 表示B原子的组成 ,
表示B原子的组成 ,