题目内容
(14分)X、Y、Z、D、E、W是原子序数依次递增的短周期主族元素。
(1)Y元素的气态氢化物与其最高价氧化物对应水化物能发生化合反应生成一种盐,该反应的化学方程式为________________________________;Y与氢原子按个数比1:2形成的含18个电子的化合物的电子式为________________。
(2)X、E同主族,纯净的单质E可用于制太阳能电池,则X在周期表中的位置是________________;X与E作电极,同NaOH溶液可构成原电池,则该电池负极的电极反应式为:______________ 。
(3)常温常压下,W的单质为气体,且常用于自来水的消毒,W的一种氧化物W2O是酸性氧化物,W2O与水反应的方程式为______________ __________________,W2O的结构式为_____________。
(4)Z、D、E、W同周期,D的简单离子半径是同周期简单离子中半径最小的, D的单质与Z的最高价氧化物对应水化物反应的离子方程式为________________________________。
(5)(XY)2与W2性质相似,则(XY)2分子中含有的化学键有_____________________(填“离子键”、“极性键”或“非极性键”);(XY)2的制备原理同实验室制取W2类似,在酸性条件下用MnO2氧化对应的阴离子得到。写出制取(XY)2的离子方程式________________________________。
(1)NH3+HNO3==NH4NO3(1分); (1分)。
(1分)。
(2)第二周期,第ⅣA族(1分);Si-4e—+6OH—==SiO32—+3H2O (2分)。
(3)Cl2O+H2O="=2HClO" (2分);Cl—O—Cl(1分)
(4)2Al+2OH—+2H2O==2AlO2—+3H2↑(2分)
(5)极性键,非极性键(2分),
MnO2+4H++2CN—==Mn2++(CN)2+2H2O (2分,(CN)2后面标或不标“↑”都不扣分;写了“△”不扣分)。
解析试题分析:根据题目中信息可以得到X、Y、Z、D、E、W六种元素分别为C、N、Na、Al、Si、Cl。
(1)Y元素的气态氢化物为NH3,最高价氧化物对应水化物为HNO3,故发生反应为:NH3+HNO3==NH4NO3
(2)C在在周期表中的位置是第二周期,第ⅣA族。C与Si作电极,同NaOH溶液构成原电池时,Si作负极失电子。
(3)Cl 2O是酸性氧化物,与水反应时生成氯元素同一价态的含氧酸。
(5)(CN)2与Cl 2性质相似为拟卤素,实验室中制取Cl 2用MnO2氧化Cl—离子得到,类比既得。
考点:本题元素化合物为载体,考查了元素周期律的应用,同时考查学生在原有知识的基础上知识的迁移、演变能力。

已知A、B、C、D、E、F、G位于元素周期表的前四周期,且元素原子序数依次增加,A焰色反应呈黄色;工业常用电解B的熔融的氯化物来制备B,C是一种能被HF和NaOH溶液溶解的单质,D的电负性比磷大,第一电离能却比磷小,E单质是制备漂白液的原料,F能形成红色(或砖红色)和黑色的两种氧化物,G是一种主族金属。
(1)前四周期所有元素中,基态原子中未成对电子与其所在周期数相同的元素有 种。
(2)元素A、B、C分别与氟气化合形成物质X、Y、Z熔点见下表:
| 氟化物 | X | Y | Z |
| 熔点/K | 1266 | 1534 | 183 |
(3)已知常温条件下,极性分子DOE2是一种液态化合物,中心原子D的杂化方式是 。向盛有10mL水的锥形瓶中滴加少量的DOE2溶液,生成两种有刺激性气味的气体。请书写此反应的化学方程式 。
(4)G与氮原子可1:1化合,形成人工合成的新型半导体材料,其晶体结构与单晶硅相似。G原子的价电子排布式为 。在该合成材料中,与同一个G原子相连的N原子构成的空间构型为正四面体。在四种基本晶体类型中,此晶体属于 晶体。
(5)F晶体的堆积方式是 (填堆积名称),其配位数为 。 向F的硫酸盐溶液中滴加氨水直至过量,写出此过程所涉及的两个离子方程式 根据价层电子对互斥理论,预测SO42-的空间构型为 。
决定物质性质的重要因素是物质的结构。请回答下列问题:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)已知:波长为300 nm的紫外光的光子,光子的能量与光的频率的关系为E=hv,式中h=6.63×10-34J·s,光的波长
 与光的频率v的关系为
与光的频率v的关系为 ,其中光速c=3×108m·s-1。根据下表有关蛋白质分子中重要化学键的信息,求波长为300 nm的紫外光的光子所具有的能量 kJ·mol-1,说明人体长时间照射紫外光后皮肤是否会受伤害的原因:
,其中光速c=3×108m·s-1。根据下表有关蛋白质分子中重要化学键的信息,求波长为300 nm的紫外光的光子所具有的能量 kJ·mol-1,说明人体长时间照射紫外光后皮肤是否会受伤害的原因: 。(未说明原因不给分)
| 共价键 | C—C | C—N | C—S |
| 键能/kJ·mol-1 | 347 | 305 | 259 |
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
(4)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 。
(5) [Cu(NH3)4]SO4中存在的化学键类型有 (填序号)。
A.共价键 B.氢键 C.离子键 D.配位键 E.分子间作用力
NH3分子的空间构型为 ,属于 分子(填“极性”或“非极性”)
 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体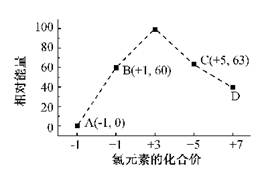
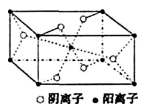

 , 试回答:
, 试回答: