题目内容
(12分)【选做题】本题包括A、B两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A.[物质结构与性质]
元素X基态原子的p电子比s电子少1个。元素Y基态原子的2p电子是2s电子的2倍。元素Z的一种单质为自然界硬度最大的物质。元素M位于第四周期,其基态原子失去3个电子后3d轨道半满。
(1)X、Y、Z的基态原子,第一电离能由大到小的顺序是 。
(2)X的氢化物易于液化,其原因是 。
(3)X与M形成的一种化合物晶胞结构如图所示。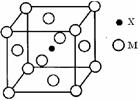
①每个晶胞中M离子的数目为 ;
②该化合物的化学式为 。
(4)Y可形成单质Y3
①Y3分子的空间构型为 (用文字描述)。
②写出一种与Y3互为等电子体的分子的化学式: 。
(5)Y、Z的化合物ZY可与M的单质生成配合物M(ZY)5,该配合物中σ键与π键的个数比为 。
(1)N>O>C (2分)(2)氨分子间形成氢键 (2分)(3)①4 ②Fe4N (各1分)
(4)①V型(或折线型) (2分)②SO2 (2分)(5)1∶1 (2分)
解析试题分析:元素X基态原子的p电子比s电子少1个,则电子排布为1s22s22p3,为N元素;元素Y基态原子的2p电子是2s电子的2倍,则2p轨道排布4个电子,为O元素;元素Z的一种单质为自然界硬度最大的物质,则元素Z为C元素;元素M位于第四周期,其基态原子失去3个电子后3d轨道半满,则M基态原子3 d轨道排布6个电子,为Fe元素。
(1)N元素2p轨道排布3个电子,为稳定状态,所以第一电离能由大到小顺序为:N>O>C
(2)N原子半径小,电负性大,氨分子间容易形成氢键,所以NH3易液化。
(3)①M位于8个顶点和6个面心,根据均摊法,每个晶胞含Fe:8×1/8+6×1/2=4。
②N原子位于晶胞中心,含有1个N原子,所以化学式为:Fe4N
(4)①O3中心O原子形成了2个O-O键,含有2对孤对电子,为sp3杂化,所以空间构型为V型(或折线型)。
②含有原子数和价电子数相等的微粒为等电子体,与O3互为等电子体的分子的化学式为SO2
(5)配合物M(ZY)5,为Fe(CO)5,含有5个σ键和5个π键,所以该配合物中σ键与π键的个数比为1:1。
考点:本题考查元素的推断、第一电离能比较、氢键、晶胞的计算、空间构型、等电子体。

 53天天练系列答案
53天天练系列答案已知A、B、C、D、E、F、G位于元素周期表的前四周期,且元素原子序数依次增加,A焰色反应呈黄色;工业常用电解B的熔融的氯化物来制备B,C是一种能被HF和NaOH溶液溶解的单质,D的电负性比磷大,第一电离能却比磷小,E单质是制备漂白液的原料,F能形成红色(或砖红色)和黑色的两种氧化物,G是一种主族金属。
(1)前四周期所有元素中,基态原子中未成对电子与其所在周期数相同的元素有 种。
(2)元素A、B、C分别与氟气化合形成物质X、Y、Z熔点见下表:
| 氟化物 | X | Y | Z |
| 熔点/K | 1266 | 1534 | 183 |
(3)已知常温条件下,极性分子DOE2是一种液态化合物,中心原子D的杂化方式是 。向盛有10mL水的锥形瓶中滴加少量的DOE2溶液,生成两种有刺激性气味的气体。请书写此反应的化学方程式 。
(4)G与氮原子可1:1化合,形成人工合成的新型半导体材料,其晶体结构与单晶硅相似。G原子的价电子排布式为 。在该合成材料中,与同一个G原子相连的N原子构成的空间构型为正四面体。在四种基本晶体类型中,此晶体属于 晶体。
(5)F晶体的堆积方式是 (填堆积名称),其配位数为 。 向F的硫酸盐溶液中滴加氨水直至过量,写出此过程所涉及的两个离子方程式 根据价层电子对互斥理论,预测SO42-的空间构型为 。
决定物质性质的重要因素是物质的结构。请回答下列问题:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)已知:波长为300 nm的紫外光的光子,光子的能量与光的频率的关系为E=hv,式中h=6.63×10-34J·s,光的波长
 与光的频率v的关系为
与光的频率v的关系为 ,其中光速c=3×108m·s-1。根据下表有关蛋白质分子中重要化学键的信息,求波长为300 nm的紫外光的光子所具有的能量 kJ·mol-1,说明人体长时间照射紫外光后皮肤是否会受伤害的原因:
,其中光速c=3×108m·s-1。根据下表有关蛋白质分子中重要化学键的信息,求波长为300 nm的紫外光的光子所具有的能量 kJ·mol-1,说明人体长时间照射紫外光后皮肤是否会受伤害的原因: 。(未说明原因不给分)
| 共价键 | C—C | C—N | C—S |
| 键能/kJ·mol-1 | 347 | 305 | 259 |
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
(4)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 。
(5) [Cu(NH3)4]SO4中存在的化学键类型有 (填序号)。
A.共价键 B.氢键 C.离子键 D.配位键 E.分子间作用力
NH3分子的空间构型为 ,属于 分子(填“极性”或“非极性”)
 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体