题目内容
8.有四种含有铝元素的化合物A、B、C、D,且能发生下列反应:①A+NaOH→D+H2O,②B$\stackrel{加热}{→}$A+H2O,③C+NaOH$\stackrel{适量}{→}$B+NaCl,
④在D溶液中通入过量CO2气体又能生成B.
(1)A、B、C、D的化学式分别是:
AAl2O3,BAl(OH)3,CAlCl3,DNaAlO2.
(2)写出对应的离子方程式:
①Al2O3+2OH-═2AlO2-+H2O;
③Al3++3OH-═Al(OH)3↓;
④AlO2-+CO2+2H2O=Al(OH)3+HCO3-.
分析 4种含有铝元素的化合物A、B、C、D,由①A+NaOH→D+H2O知,化合物A和强碱反应生成D和水,所以A是Al(OH)3或Al2O3,那么D是NaAlO2;由②B$\stackrel{加热}{→}$A+H2O,A是Al2O3,B是Al(OH)3;由③C+NaOH$\stackrel{适量}{→}$B+NaCl知,B是Al(OH)3,根据元素守恒得,C是AlCl3,以此解答该题.
解答 解:4种含有铝元素的化合物A、B、C、D,由①A+NaOH→D+H2O知,化合物A和强碱反应生成D和水,所以A是Al(OH)3或Al2O3,那么D是NaAlO2;由②B$\stackrel{加热}{→}$A+H2O,A是Al2O3,B是Al(OH)3;由③C+NaOH$\stackrel{适量}{→}$B+NaCl知,B是Al(OH)3,根据元素守恒得,C是AlCl3,
(1)根据上面分析可知,A是Al2O3,B是Al(OH)3,C是AlCl3,D是NaAlO2,
故答案为:Al2O3;Al(OH)3;AlCl3;NaAlO2;
(2)反应①的离子方程式为Al2O3+2OH-═2AlO2-+H2O,③的离子方程式为Al3++3OH-═Al(OH)3↓,④的离子方程式为AlO2-+CO2+2H2O=Al(OH)3+HCO3-;
故答案为:NaAlO2;AlO2-+2OH-═2AlO2-+H2O;Al3++3OH-═Al(OH)3↓;AlO2-+CO2+2H2O=Al(OH)3+HCO3-;
点评 本题考查无机物的推断,题目难度不大,注意以A是含铝元素的化合物且和强碱反应生成水作突破口判断A和D;利用倒推法再根据②中的方程式判断B;再利用倒推法结合元素守恒判断C,从而得出答案.

练习册系列答案
相关题目
19.下列叙述正确的是( )
| A. | 合成高分子材料都难以降解,会造成环境污染 | |
| B. | 塑料、涂料和合成橡胶被称为“三大合成材料” | |
| C. | 食品包装袋、食物保鲜膜等材料的主要成分是聚氯乙烯 | |
| D. | 用于生产“尿不湿”的高吸水性树脂属于功能高分子材料 |
16.下列离子方程式正确的是( )
| A. | 氨水和盐酸反应:OH-+H+═H2O | |
| B. | 稀硫酸中滴加氢氧化钡溶液:H++OH-═H2O | |
| C. | 碳酸钙中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| D. | 锌与硫酸铜溶液反应:Zn+Cu2+═Zn2++Cu |
3.A、B、C、D、E均为短周期元素,且原子序数依次增大,请根据表中信息回答下列问题:
(1)E在元素周期表中的位置第三周期第ⅥA族.
(2)B最简单气态氢化物的电子式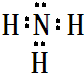 ,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式
,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式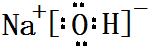 ,所含化学键类型:离子键、共价键.
,所含化学键类型:离子键、共价键.
(3)B、C、D、E简单离子半径由大到小顺序为:S2->N3->O2->Na+(填元素符号).
(4)用电子式表示E的氢化物的形成过程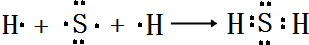 .
.
(5)由A、B、C与氢元素组成的一种常见酸式盐与过量D的最高价氧化物的水化物反应的离子方程式:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
(6)19.2g金属铜与一定浓度的B的最高价氧化物的水化物反应,产生标准状况下NO、NO2(不考虑N2O4的存在)混合气6.72L,则参加反应的HNO3的物质的量为0.9mol.
| 元素 | 元素性质或结构 |
| A | 最外层电子数是其内层电子数的2倍 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D元素在同周期中金属性最强 |
| E | 常温常压下,E元素形成的单质是淡黄色固体,常在火山口附近沉积 |
(2)B最简单气态氢化物的电子式
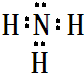 ,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式
,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式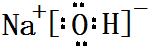 ,所含化学键类型:离子键、共价键.
,所含化学键类型:离子键、共价键.(3)B、C、D、E简单离子半径由大到小顺序为:S2->N3->O2->Na+(填元素符号).
(4)用电子式表示E的氢化物的形成过程
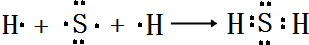 .
.(5)由A、B、C与氢元素组成的一种常见酸式盐与过量D的最高价氧化物的水化物反应的离子方程式:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
(6)19.2g金属铜与一定浓度的B的最高价氧化物的水化物反应,产生标准状况下NO、NO2(不考虑N2O4的存在)混合气6.72L,则参加反应的HNO3的物质的量为0.9mol.
13.当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A. | 稀硫酸 | B. | Cu(NO3)2 溶液 | C. | 汽油、水混合物 | D. | Fe(OH)3胶体 |
20.下列各种叙述中,正确的是( )
①Cl-和Cl2的性质相同 ②ClO-具有氧化性 ③Cl-比Cl多一个电子 ④盐酸兼有酸性、氧化性、还原性 ⑤Cl-具有酸性 ⑥Cl2的氧化性比MnO2的强 ⑦Cl2只有氧化性而没有还原性.
①Cl-和Cl2的性质相同 ②ClO-具有氧化性 ③Cl-比Cl多一个电子 ④盐酸兼有酸性、氧化性、还原性 ⑤Cl-具有酸性 ⑥Cl2的氧化性比MnO2的强 ⑦Cl2只有氧化性而没有还原性.
| A. | ①②⑤⑥ | B. | 仅②④⑥ | C. | 仅②③④ | D. | ②③④⑥ |
17.某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究,实验过程如图,下列说法不正确的是( )

| A. | ①和②都是过滤操作 | |
| B. | 滤渣的成分是Cu和Fe的混合物 | |
| C. | 操作③和④都是在蒸发皿中进行 | |
| D. | 溶液B中反应的离子方程式:4Fe2++O2+8NH3+10H2O═8NH4++4Fe(OH)3↓ |
18.下列离子方程式书写正确的是( )
| A. | Cl2和水反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Fe加入CuSO4溶液:2Fe+3Cu2+═2Fe3++3Cu | |
| C. | AlCl3溶液中加入氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 石灰石溶于稀盐酸:CaCO3+2H+═Ca2++H2O+CO2↑ |
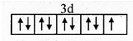 .
.