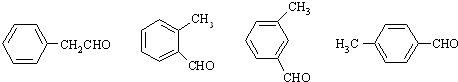
题目内容
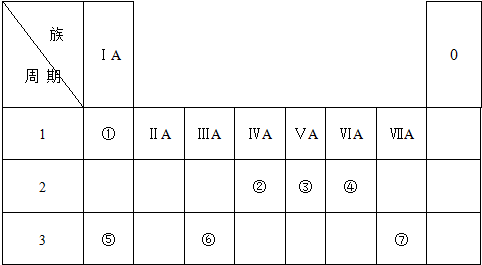
12.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的是:KOH.
(3)最高价氧化物是两性氧化物的元素是Al;写出它的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(4)用电子式表示元素④与⑥的化合物的形成过程:
 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.(5)元素的气态氢化物中成碱性的物质是NH3,该元素氢化物与其最高价氧化物对应水化物反应的化学方程式为NH3+HNO3=NH4NO3.
分析 根据元素在周期表中的相对位置推知:①是C,②是N,③是O,④是Na,⑤是Al,⑥是S,⑦是Cl,⑧是Ar,⑨是K,
(1)稀有气体化学性质稳定;氩原子的核电荷数=核外电子总数=18,最外层达到8电子稳定结构;
(2)同周期元素的原子,从左到右最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱,同主族元素的原子,从下到上最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱;
(3)氢氧化铝是两性氢氧化物,能和强碱反应生成盐和水;
(4)硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物;
(5)气态氢化物呈碱性的为氨气,氮元素的最高价氧化物为硝酸,硝酸与氨气反应生成硝酸铵.
解答 解:根据元素在周期表中的相对位置推知:①是C,②是N,③是O,④是Na,⑤是Al,⑥是S,⑦是Cl,⑧是Ar,⑨是K,
(1)在这些元素中,化学性质最稳定的是稀有气体Ar;氩的原子序数为18,其最外层为8电子稳定结构,其原子结构示意图为: ,
,
故答案为:Ar; ;
;
(2)根据元素周期律:同周期元素的原子,从左到右最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱,同主族元素的原子,从下到上最高价氧化物对应水化物的酸性逐渐增强,碱性逐渐减弱可以推知酸性最强的式是高氯酸,碱性最强的是KOH,
故答案为:HClO4;KOH;
(3)氢氧化铝是两性氢氧化物,所以最高价氧化物是两性氧化物的元素是Al,能和强碱反应生成盐和水,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al;Al(OH)3+OH-=AlO2-+2H2O;
(4)硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为: ,
,
故答案为: ;离子;
;离子;
(5)氢化物为碱性的气体为氨气,化学式为NH3,氮元素的最高价氧化物为硝酸,硝酸与氨气反应生成硝酸铵,反应的化学方程式为:NH3+HNO3=NH4NO3,
故答案为:NH3;NH3+HNO3=NH4NO3.
点评 本题考查了元素周期表和元素周期律的综合应用,题目难度中等,熟练掌握元素周期表结构、元素周期律的内容为解答关键,还要明确常见化学用语的表示方法、化学方程式的书写原则等知识,试题充分考查了学生灵活应用基础知识解决实际问题的能力.

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案| A. | NH3属于离子化合物 | |
| B. | 常温下,液氨的电离平衡常数为10-14 | |
| C. | 液态氨与氨水的组成相同 | |
| D. | 液氨中的微粒含相同的电子数 |
| A. | 加成反应 | B. | 消去反应 | C. | 取代反应 | D. | 氧化反应 |
| IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是K,单质常温下是液体的元素是Br;
(3)表中能形成两性氢氧化物的元素是Al,分别写出该元素的最高氧化物的水化物与⑥、⑨最高价氧化物的水化物反应的离子方程式:Al(OH)3+3H+=Al3++3H2O,Al(OH)3+OH-=AlO2-+2H2O;
(4)写出一个离子方程式,比较⑦、⑩单质氧化性的强弱:Cl2+2Br-=Br2+2Cl-.
| A. | 两种不同元素的原子 | B. | 两种不同元素的离子 | ||
| C. | 两种不同分子 | D. | 两种元素的原子和离子 |
 (任选一种).
(任选一种).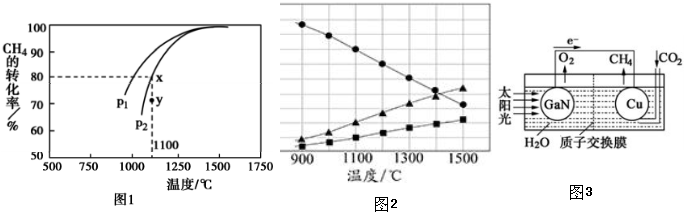
 ,③与①所形成的化合物的结构式为:
,③与①所形成的化合物的结构式为: .
. .
.