题目内容
7.下表为元素周期表的一部分,请回答有关问题:| IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是K,单质常温下是液体的元素是Br;
(3)表中能形成两性氢氧化物的元素是Al,分别写出该元素的最高氧化物的水化物与⑥、⑨最高价氧化物的水化物反应的离子方程式:Al(OH)3+3H+=Al3++3H2O,Al(OH)3+OH-=AlO2-+2H2O;
(4)写出一个离子方程式,比较⑦、⑩单质氧化性的强弱:Cl2+2Br-=Br2+2Cl-.
分析 (1)根据元素周期表,可确定①、②、③、④、⑤、⑥、⑦、⑧、⑨、⑩元素分别为:N、F、Mg、Al、Si、S、Cl、Ar、K、Br;
(2)又知金属性:同周期从左到右越来越小,同主族从上到下越来越大;而非金属性:同周期从左到右越来越大,同主族从上到下越来越小;
(3)氢氧化铝为两性化合物,既能与酸反应,又能与碱反应;
(4)利用“在氧化还原反应中,氧化剂氧化性大于氧化产物”原理,设计反应Cl2+2NaBr=2NaCl+Br2.
解答 解:①、②、③、④、⑤、⑥、⑦、⑧、⑨、⑩元素分别为:N、F、Mg、Al、Si、S、Cl、Ar、K、Br;
(1)⑧为元素氩Ar;硅单质为原子晶体,故答案为:Ar;Si;
(2)表中最活泼的金属应从元素周期表的左下角去找⑨应为元素钾K,常温下呈现液体状态的是溴(Br),故答案为:K;Br;
(3)表中能形成两性氢氧化物的元素是④元素铝Al,⑥元素为S最高价氧化物的水化物为H2SO4,它与Al(OH)3反应的离子方程式为:Al(OH)3+3H+=Al3++3H2O,与氢氧化钾反应生成偏铝酸钾和水,离子反应方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al;Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(4)元素⑦为氯,元素⑩为溴,氯单质将溴离子氧化为溴单质就能证明氯化溴的氧化性强.将氯水加入到溴化钠溶液中,有红棕色的Br2生成,证明单质氯比单质溴氧化性强,离子反应方程式为:Cl2+2Br-=Br2+2Cl-,故答案为:Cl2+2Br-=Br2+2Cl-.
点评 本题考查元素周期表与元素周期律的综合应用,难度不大,侧重学生对基础知识的巩固.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
2.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1 mol过氧化钠中阴离子所带的负电荷数为NA | |
| B. | 14g乙烯和丙烯的混合物中含有的碳原子的数目为NA | |
| C. | 28g C18O与28g C16O中含有的质子数均为14NA | |
| D. | 标准状况下,22.4L氯气与足量的氢氧化钠溶液反应转移的电子数目为2NA |
19.在反应A+2HCl═MgCl2+2B中A可能是下列物质中的( )
| A. | Mg | B. | MgO | C. | Mg(OH)2 | D. | MgCO3 |
12.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号或化学式,下同).原子结构示意图为 .
.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的是:KOH.
(3)最高价氧化物是两性氧化物的元素是Al;写出它的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(4)用电子式表示元素④与⑥的化合物的形成过程: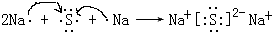 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.
(5)元素的气态氢化物中成碱性的物质是NH3,该元素氢化物与其最高价氧化物对应水化物反应的化学方程式为NH3+HNO3=NH4NO3.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的是:KOH.
(3)最高价氧化物是两性氧化物的元素是Al;写出它的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(4)用电子式表示元素④与⑥的化合物的形成过程:
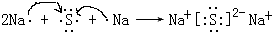 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.(5)元素的气态氢化物中成碱性的物质是NH3,该元素氢化物与其最高价氧化物对应水化物反应的化学方程式为NH3+HNO3=NH4NO3.
19.根据元素周期表和元素周期律,下列推断中错误的是( )
| A. | 砹是一种有色固体,它的气态氢化物很不稳定 | |
| B. | F2与水反应比Cl2与水反应剧烈 | |
| C. | 铷的最高价氧化物的水化物一定是强碱 | |
| D. | 由盐酸的酸性比氢硫酸强可推知氯的非金属性强于硫 |
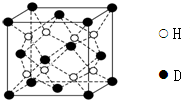 已知A、B、C、D、E、F、G、H、I为元素周期表中原子序数依次增大的前四周期元素,A原子的最外层中p轨道上的电子数等于前一电子层电子总数;A、B、C、D;E、F与G分别位于同一周期.C原子L层上有2对成电子,D、E、F的核外电子排布相同的简单离子可形成一种E3FD6型离子晶体X,EG、HC为电子数相同的离子晶体.I原子M层为全充满状态,且核外的未成对电子只有一个.请根据以上情况,回答下列问题:(答题时,用对应的元素符号表示)
已知A、B、C、D、E、F、G、H、I为元素周期表中原子序数依次增大的前四周期元素,A原子的最外层中p轨道上的电子数等于前一电子层电子总数;A、B、C、D;E、F与G分别位于同一周期.C原子L层上有2对成电子,D、E、F的核外电子排布相同的简单离子可形成一种E3FD6型离子晶体X,EG、HC为电子数相同的离子晶体.I原子M层为全充满状态,且核外的未成对电子只有一个.请根据以上情况,回答下列问题:(答题时,用对应的元素符号表示)