题目内容
7.有机物W与CH3COOH无论以何种比例混合只要质量一定,完全燃烧后产生水的质量也一定,试回答:(1)符合条件的W的必要条件是有机物W中氢元素质量分数为为$\frac{1}{15}$.
(2)符合条件的分子量最小的有机物W的结构简式是HCHO.
(3)若W与乙酸相对分子质量相等,则W的结构简式可以是HCOOCH3.
(4)若W中C、H元素质量分数之和为86.67%,其余为氧,W的相对分子质量小于200,则W的分子式为C8H8O;如果W中含苯环结构且能发生银镜反应,符合条件的W的同分异构体有4种,任写一种结构简式:
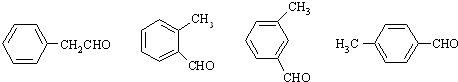 (任选一种).
(任选一种).
分析 (1)有机物W(含C、H、O三种元素)与CH3COOH无论以何种比例混合,只要混合物总质量不变,完全燃烧后产生的水的质量也不变,说明H元素质量分数为定值,则有机物W中氢元素质量分数为$\frac{1}{15}$;
(2)CH3COOH的最简式为CH2O,与甲醛的分子式相同;
(3)W与乙酸的相对分子质量相等,可能为乙酸的同分异构体甲酸甲酯;
(4)计算氧元素的质量分数,进而计算氧原子最大数目,确定含有O原子数目,再计算有机物的相对分子质量,进而计算分子中H、C原子数数目,确定分子式;如果W中含苯环结构且能发生银镜反应,则含有醛基或为甲酸形成的酯,结合有机物的分子式确定其结构.
解答 解:(1)有机物W(含C、H、O三种元素)与CH3COOH无论以何种比例混合,只要混合物总质量不变,完全燃烧后产生的水的质量也不变,则有机物W中氢元素质量分数为$\frac{1}{15}$,
故答案为:有机物W中氢元素质量分数为为$\frac{1}{15}$;
(2)CH3COOH的最简式为:CH2O,与甲醛的分子式相同,故符合条件的相对分子量最小的有机物W为HCHO,
故答案为:HCHO;
(3)若W与乙酸相对分子质量相等,则W可能与乙酸互为同分异构体,如:甲酸甲酯,其结构简式为:HCOOCH3,
故答案为:HCOOCH3;
(4)氧元素的质量分数=1-86.67%=13.33%,W的相对分子量小于200,W分子中最大氧原子数目=$\frac{200×13.33%}{16}$=1.7,故W含有1个氧原子,则W的相对分子质量为:$\frac{16}{13.33%}$=120,则W分子中N(H)=$\frac{120×\frac{1}{15}}{1}$=8,N(C)=$\frac{120-16-8}{16}$=8,故W的分子式为:C8H8O;
如果W中含苯环结构且能发生银镜反应,符合条件的W的同分异构体有 ;
;
故答案为:C8H8O;4; (任选一种).
(任选一种).
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,注意掌握确定有机物分子式常用方法,明确同分异构体的概念及书写原则,试题侧重考查学生的分析、理解能力.

 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案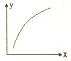 MgO可以通过下列反应制备:MgSO4(s)+CO(g)?MgO(s)+CO2(g)+SO2(g)△H>0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
MgO可以通过下列反应制备:MgSO4(s)+CO(g)?MgO(s)+CO2(g)+SO2(g)△H>0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( ) | 选项 | x | y |
| A | CO的物质的量 | CO与CO的物质的量之比 |
| B | SO的浓度 | 平衡常数K |
| C | 温度 | 容器内混合气体的密度 |
| D | CO的浓度 | CO的转化率 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大 | |
| B. | 向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp减小 | |
| C. | 向0.0008mol/L的K2CrO4溶液中加入等体积的0.002mol/LAgNO3溶液,则CrO42-完全沉淀 | |
| D. | 将0.001mol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001mol/L的K2CrO4溶液,则先产生AgCl沉淀 |
| A. | 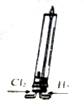 该装置可模拟工业制取氯化氢 | |
| B. | 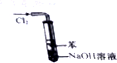 如图实验装置可以处理Cl2尾气,并防止倒吸 | |
| C. |  如图实验制取少量的Fe(OH)3胶体 | |
| D. | 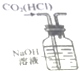 如图实验装置可除去CO2气体中含有的少量HCl杂质 |
| A. | 1 mol过氧化钠中阴离子所带的负电荷数为NA | |
| B. | 14g乙烯和丙烯的混合物中含有的碳原子的数目为NA | |
| C. | 28g C18O与28g C16O中含有的质子数均为14NA | |
| D. | 标准状况下,22.4L氯气与足量的氢氧化钠溶液反应转移的电子数目为2NA |
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
| A. | Mg | B. | MgO | C. | Mg(OH)2 | D. | MgCO3 |
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的是:KOH.
(3)最高价氧化物是两性氧化物的元素是Al;写出它的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
(4)用电子式表示元素④与⑥的化合物的形成过程:
 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.(5)元素的气态氢化物中成碱性的物质是NH3,该元素氢化物与其最高价氧化物对应水化物反应的化学方程式为NH3+HNO3=NH4NO3.
| 稀盐酸的质量 | 剩余固体的质量 |
| 第1次加入5g | 1.315g |
| 第2次加入5g | 0.63g |
| 第3次加入5g | 0.3g |
| 第4次加入5g | 0.3g |
(2)石灰石样品的纯度为;
(3)100Kg这种纯度的石灰石充分煅烧后,可得到固体多少克?