题目内容
11.下列各组物质中,都是共价化合物的是( )| A. | H2O2和CaF2 | B. | H2S和Na2O2 | C. | HNO3和HClO4 | D. | NH3和N2 |
分析 含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,据此分析解答.
解答 解:A.双氧水分子中只含共价键为共价化合物,氟化钙中只含离子键,为离子化合物,故A错误;
B.硫化氢只含共价键,为共价化合物,过氧化钠中含有离子键和共价键,为离子化合物,故B错误;
C.硝酸和高氯酸中都只含共价键,为共价化合物,故C正确;
D.氮气为单质不是化合物,故D错误;
故选C.
点评 本题考查离子化合物和共价化合物的判断,侧重考查基本概念,明确化合物和化学键的关系是解本题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.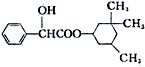 环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )
环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )
 环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )
环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )| A. | 该物质属于芳香烃 | |
| B. | 该有机物不能被氧化成醛 | |
| C. | 分子式为C17H23O3 | |
| D. | 1mol该物质最多可与2 mol NaOH发生反应 |
16.对于可逆反应4NH3+5O2?4NO+6H2O(g),下列叙述正确的是( )
| A. | 只有达到平衡时,消耗O2的速率与生成NO的速率之比才为5;4 | |
| B. | 若单位时间生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 | |
| C. | 达到平衡状态后,NH3、O2、NO、H2O(g)的物质的量保持不变 | |
| D. | 达到平衡状态时,若增加容器体积,则反应速率增大 |
14.将洁净的金属片Fe、Zn、A、B 分别与Cu用导线连结浸在合适的电解质溶液里.实验并记录电压指针的移动方向和电压表的读数如下表所示.根据以上实验记录,完成以下填空:
①构成两电极的金属活动性相差越大,电压表的读数越大(填“大”、“小”).上述五种金属的金属性由强到弱的顺序是Zn>Fe>B>Cu>A.
②Cu与A组成的原电池,Cu为负极,此电极反应式为Cu-2e-=Cu2+.
③A、B形成合金,露置在潮湿空气中,B先被腐蚀.
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe→Cu | +0.78 |
| Zn | Zn→Cu | +1.10 |
| A | A←Cu | -0.15 |
| B | B→Cu | +0.3 |
②Cu与A组成的原电池,Cu为负极,此电极反应式为Cu-2e-=Cu2+.
③A、B形成合金,露置在潮湿空气中,B先被腐蚀.
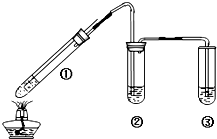 某小组用图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.
某小组用图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.
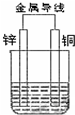
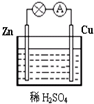 (1)Zn极为原电池的负(填“正”或“负”)极,该极的电极反应式是Zn-2e-=Zn2+,属于氧化反应(填“氧化反应”或“还原反应”).Cu极的电极反应式是2H++2e-=H2↑,
(1)Zn极为原电池的负(填“正”或“负”)极,该极的电极反应式是Zn-2e-=Zn2+,属于氧化反应(填“氧化反应”或“还原反应”).Cu极的电极反应式是2H++2e-=H2↑, (1)NF3分子中N原子的杂化轨道类型为sp3,该分子的空间构型为三角锥形
(1)NF3分子中N原子的杂化轨道类型为sp3,该分子的空间构型为三角锥形